下列说法或做法正确的是
A CO2通入可溶性硅酸盐中析出硅酸沉淀,所以硅酸的酸性小于碳酸
B 金属钠着火燃烧时,用泡沫灭火器灭火
C 铝比铁活泼,所以铝比铁更容易被腐蚀
D 正常雨水PH等于7,酸雨的PH小于7
设NA为阿伏加德罗常数的值。下列说法正确的是
| A.46g乙醇中含有的C—H键的数目为6NA |
| B.0.lmol丙烯酸中含有的双键的数目为0.lNA |
| C.1mol甲基(—CH3)中含有的电子总数为9NA |
| D.标准状况下,22.4L己烷完全燃烧生成的CO2分子的数目约为6NA |
下列有关物质性质或用途的说法不正确的是
| A.乙醇能够使蛋白质变性,75%(体积分数)的乙醇溶液可用于医疗消毒 |
| B.乙二醇的水溶液凝固点很低,可用作汽车发动机的抗冻剂 |
| C.光照时乙烷与氯气能发生取代反应,工业上常用该反应生产氯乙烷 |
| D.油脂的碱性水解又称为皂化,其产物之一高级脂肪酸盐可用于制造肥皂 |
下列关于有机化合物的认识中,正确的是。、
| A.分子式为C4H10O的醇共有4种 |
| B.包装用的材料聚乙烯和聚氯乙烯都属于烃 |
| C.乙酸(CH3COOH)与油酸(C17H33COOH)互为同系物 |
| D.淀粉、纤维素的分子式都是(C6H10O5)n,二者互为同分异构体 |
下列有机物与其名称相符的是
A.3,3—二甲基丁烷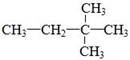 |
| B.l—丁烯:CH2=CH—CH2—CH3 |
C.间二甲苯: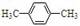 |
D.苯甲醇: |
下列有关化学用语表示正确的是
A.羟基的电子式: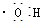 |
B.乙炔的结构式:CHCH |
C.硝基苯的结构简式: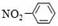 |
D.甲烷分子的球棍模型: |