(15分)
我国有丰富的天然气资源。以天然气为原料合成尿素的主要步骤如下图所示(图中某
些转化步骤及生成物未列出):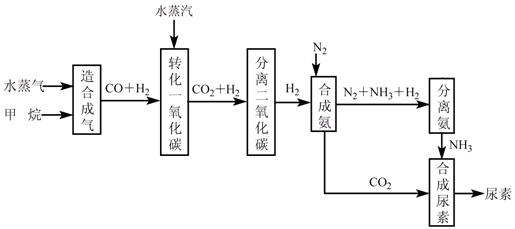
请填写下列空白:
(1)已知0.5 mol甲烷和0.5 mol水蒸气在t ℃,p k Pa时,完全反应生成一氧化碳和氢气(合成气),吸收了a kJ热量。该反应的热化学方程式是: ______。
(2)上述流程中,工业上分离H2、CO2合理的方法是___________。
| A.混合气先通入氢氧化钠溶液,再在溶液中加盐酸 |
| B.混合气加压冷却,使CO2液化 |
| C.混合气用氨水洗涤 |
| D.混合气先通入到石灰浆,然后高温煅烧固体, |
(3)为了保证氨气顺利合成,在空气进入合成塔之前必须对空气进行___________,目的是________________________________________;在合成氨的实际生产过程中,常采取将生成的氨从混合气体中分离出来,分离出氨的方法: 。
(4)合理地利用资源不仅可以提高经济效益,而且也是对社会、对全人类负责的表现,请用线段和箭头画出图中的两处合理利用资源情况。
化合物A、D、F是中学化学中常见的物质,化合物B、C、E中含有两种相同的元素。这些化合物之间存在如下图的转化关系。其中A和B的反应是一种重要化工生产中的主要反应之一。
(1)在化合物A、C、F中含有相同的元素是________________。
(2)化合物C的化学式是________________。
(3)化合物C的水溶液和化合物D能否发生反应?,其理由是_________________________
______________________________________________________________________________。
GaAs(砷化镓)是仅次于硅的一种新型化合物半导体材料,其性能比硅更优越。Ga位于周期表的第ⅢA族,As位于周期表的第ⅤA族。
(1)Ga和As的最外层电子数分别是:Ga________、As________。
(2)GaAs中Ga和As的化合价分别是:Ga________价、As________价。
(3)第ⅣA族的C和Si也可以形成类似的化合物半导体材料,该化合物半导体材料的化学式可表示为________。
2005年10月12日“神舟六号”载人飞船成功发射,是我国航天史上又一座新的里程碑,标志着我国在攀登世界科技高峰的征程上,又迈出了具有重大历史意义的一步。
(1)“神舟六号”飞船表面贴有特制的陶瓷片,其主要目的是_____________________。
(2)航天员采用的补氧剂有Na2O2、KO2两种选择,写出反应原理____________________。
(3)1 kg Na2O2与1 kg KO2分别与CO2反应,生成O2的体积(同温、同压)之比为_______。
(4)你认为选用_______作补氧剂更为合适,理由是:
框图中,A、B、C是单质,甲、乙、丙等是化合物;物质中所包含的元素都是短周期元素。
试完成下列问题:
(1)写出A、B、C的化学式:__________、__________、__________。
(2)写出甲、丙、己的化学式:__________、__________、__________。
(3)框图所列单质和化合物中,含有碳元素的是_________(写字母代号或汉字代号)。
铁氧体磁性材料在微波领域中有着重要作用,有一种铁、氧、钇三种元素组成的磁性材料,经测定该材料中钇、铁原子数之比为3∶5,氧的质量分数约为26.0%,则该材料的化学式为,钇、铁的化合价分别为。