(每空3分,共12分)常温下,将3种一元酸分别和NaOH溶液等体积混合,实验数据如下: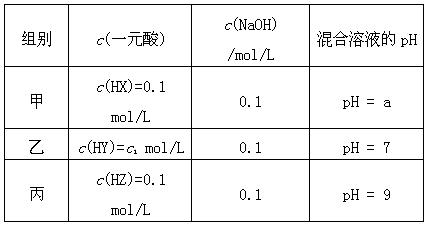
(1)甲组实验中HX为弱酸,a______7(填“<”,“=”或“>”)。
(2)乙组实验中HY为强酸,则HY溶液的pH= 。
(3)丙组实验发生反应的离子方程式为 ,
所得溶液中由水电离出的c(OH-) = mol/L。
某烃A、B的分子式均为C6H10,它们的分子结构中无支链或侧链。
(1)A为环状化合物,它能与Br2发生加成反应,A的名称是________。
某烯烃1 mol与H2加成后产物为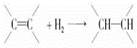 ,则原烯烃可能的结构简式为________________________。
,则原烯烃可能的结构简式为________________________。
CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是________。
(2)120 ℃、101 kPa下,a mL由CO、CH4组成的混合气体在b mL O2中完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生b mL CO2,则混合气体中CH4的体积分数为____________(保留2位小数)。
②若燃烧后气体体积缩小了a/4 mL,则a与b关系的数学表示式是_____________。
已知萘是最简单的稠环芳香烃,其分子式为C10H8,结构式则可以看成为两个苯环共用两个相邻的碳原子,故它在化学性质上与苯有许多类似之处,现有一定量的萘,在一定条件下可以发生下列转化:
(1)请写出C10H7SO3H可能的结构简式:_____________________。
(2)写出发生反应的化学方程式__________________________________________________。
请认真阅读下列三个反应:
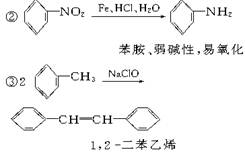
利用这些反应,按以下步骤可从某烃A合成一种染料中间体DSD酸。(试剂和条件已略去)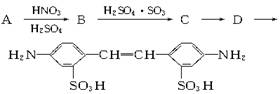
请写出A、B、C、D的结构简式。
A_______________; B______________C___________;D_________________。