下表中的实验操作能达至实验目的或得出相应结论的是 ( )
| 选项 |
实验操作 |
实验目的或结论 |
| A |
某实验得到热化学方程式: S(l)+O2(g)=SO2(g);ΔH=-293.23kJ/mol |
1molSO2的键能的总和小于1mol硫和1mol氧气的键能之和 |
| B |
C2H5Br与NaOH溶液混合充分振荡,再加入AgNO3溶液 |
检验C2H5Br中的溴元素 |
| C |
向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 |
说明溶液中一定含有Fe2+ |
| D |
将少量某物质滴加到新制的氢氧化铜悬浊液中,加热后有红色沉淀生成 |
说明该物质一定是醛 |
.硫酸铝、硫酸钾、明矾三种物质组成的混和物中,当SO42-的浓度为0.20mol/L时,加入等体积的0.20mol/L的KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的浓度是
| A.0.20mol/L | B.0.25mol/L | C.0.225mol/L | D.0.45mol/L |
.能用离子方程式H+ + OH = H2O表示的化学反应是
| A.NaOH溶液和醋酸的反应 | B.Ba(OH)2溶液和稀H2SO4的反应 |
| C.NaOH溶液和硫酸氢钠溶液反应 | D.氨水和稀H2SO4的反应 |
下列实验方案设计合理的是
| A.鉴别氯化铝和氯化镁溶液:分别滴加过量的氢氧化钠溶液 |
| B.除去氯化铵溶液中的氯化铁:向溶液中滴加适量氢氧化钠溶液,过滤 |
| C.除去苯中的苯酚:向溶液中加入浓溴水,过滤 |
| D.检验溴乙烷中的溴元素:在溴乙烷中滴入氢氧化钾溶液加热后,再滴加硝酸银溶液 |
.下列实验操作完全正确的是
| 编号 |
实验 |
操作 |
| A |
容量瓶查漏 |
加水、倒立、观察、正立 |
| B |
配制一定浓度的氯化钾溶液1000mL |
准确称取氯化钾固体,放入到1000ml的容量瓶中,加水溶解,振荡摇匀,定容 |
| C |
为确证NaHCO3固体中是否含Na2CO3 |
取少量待检固体溶于水中,滴加少量BaC12溶液,观察是否有白色沉淀生成 |
| D |
取出分液漏斗中所需的上层液体 |
下层液体从分液漏斗下端管口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 |
常温下,下列各组离子,在所给条件下能够大量共存的是
A.pH=0的溶液中,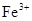 、 、 、 、 、 、 |
B.水电离出的c(H+)=1×1010的溶液中,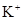 、 、 、Na+、 、Na+、 |
C.使pH试纸显深蓝色的溶液中,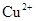 、 、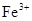 、 、 、 、 |
D.在 溶液中 溶液中 、SiO32-、NH4+、 、SiO32-、NH4+、 . . |