门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是:
| A.X单质不易与水反应 | B.XO2可被碳或氢还原为X |
| C.XCl4的沸点比SiCl4的高 | D.XH4的稳定性比SiH4的高 |
乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为CH2=C=O+HA → CH3—CO—A。乙烯酮在一定条件下可与下列试剂加成,其产物不正确的是
A.与HCl加成生成CH3COCl
B.与H2O加成生成CH3COOH
C.与CH3COOH加成生成CH3COOCOCH3
D.与CH3OH加成生成CH3COCH 2OH
2OH
在国际环境问题中,使用由聚苯乙烯材料做成的各种制品,由于难以分解,处理麻烦而带来“白色污染”。最近研制出一种新材料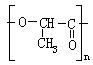 代替聚苯乙烯,它是由乳酸缩聚而生成的,该种材料可在乳酸菌作用下发生降解,从而消除对环境的污染。下列关于聚乳酸或乳酸的说法正确的是
代替聚苯乙烯,它是由乳酸缩聚而生成的,该种材料可在乳酸菌作用下发生降解,从而消除对环境的污染。下列关于聚乳酸或乳酸的说法正确的是
| A.聚乳酸是一种纯净物 |
| B.其聚合方式与聚苯乙烯相似 |
C.聚乳酸的单体为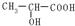 |
| D.乳酸在一定条件下能被氧化为二元羧酸 |
反应C(s)+H2O(g)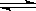 CO(g)+ H2(g),△H>0,在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应平衡状态几乎无影响的是
CO(g)+ H2(g),△H>0,在一可变容积的密闭容器中进行,在其它条件不变的情况下,下列条件的改变对其反应平衡状态几乎无影响的是
| A.增加C的物质的量 |
| B.将容器的体积缩小一半 |
| C.给容器升高温度 |
| D.保持压强不变,充入N2使容器体积变大 |
同学甲对某基态原子的价电子排布式书写为nS2nP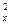 P
P P
P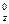 ,你认为同学甲所书写的电子排布式违背了下列选项中的
,你认为同学甲所书写的电子排布式违背了下列选项中的
| A.能量最低原理 | B.泡利不相容原理 |
| C.洪特规则 | D.洪特的全充满、半充满、全空状态 |
某元素原子的价电子构型为2s22p5的元素,与其同周期元素相比,下列有关描述中正确的有
| A.原子序数为7 | B.电负性最大 |
| C.原子半径最大 | D.第一电离能最大 |