取10 mL 0.4 mol·L-1 FeCl3溶液置于烧杯中,向其中加入一定量的Fe、Cu混合物充分反应。下列叙述中一定不正确的是(设溶液体积不变,不考虑水解因素)
| A.烧杯中有Cu无Fe,反应后溶液中c(Fe2+)≤0.6 mol·L-1 |
| B.烧杯中有Fe无Cu,反应后溶液中c(Fe2+)=0.6 mol·L-1 |
| C.烧杯中Fe、Cu均无,反应后溶液中c(Cl-)=1.2 mol·L-1 |
D. 烧杯中Fe、Cu均有,反应后溶液中c(Fe2+)=0.6 mol·L-1 烧杯中Fe、Cu均有,反应后溶液中c(Fe2+)=0.6 mol·L-1 |
下列实验所采取的分离方法与对应原理都正确的是
| 选项 |
目的 |
分离方法 |
原理 |
| A |
提取碘水中的碘 |
乙醇萃取 |
碘在乙醇中溶解度比水中大 |
| B |
除去纯碱中的碳酸氢铵 |
加热 |
纯碱热稳定性大于碳酸氢铵 |
| C |
分离KNO3和NaCl |
重结晶 |
KNO3的溶解度大于NaCl |
| D |
分离乙酸乙酯和乙醇 |
分液 |
乙酸乙酯密度大于乙醇 |
下列关于右图所示转化关系(X代表卤素)的说法错误的是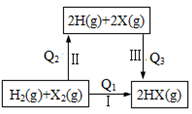
| A.Q3>0 | B.Q1=Q2 + Q3 |
| C.按Cl、Br、I的顺序,Q2依次增大 | D.Q1越大,HX越稳定 |
可以描述两种一元酸:甲( Ki=1.8×10-5)和乙( Ki=1.4×10-3)在水中的电离度与浓度关系的曲线是
A. |
B.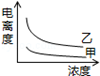 |
C.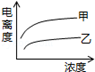 |
D.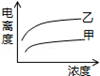 |
在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如下图所示,下列说法正确的是
| A.外电路的电流方向为:X→外电路→Y |
| B.X极上发生的是还原反应 |
| C.溶液中氢离子向X极移动 |
| D.若两电极都是金属,则它们的活动性顺序为X>Y |
已知:
(1)Al(OH)3的电离方程式为:AlO2-+H++H2O Al(OH)3
Al(OH)3 Al3++3OH-
Al3++3OH-
(2)无水AlCl3晶体的沸点为182.9℃,溶于水的电离方程式为:AlCl3 → Al3++3Cl-
(3)PbSO4难溶于水,易溶于CH3COONa溶液,反应的化学方程式为:
PbSO4+2CH3COONa→Na2SO4+(CH3COO)2Pb
下列关于Al(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是
| A.均为共价化合物 | B.均为离子化合物 |
| C.均为强电解质 | D.均为弱电解质 |