下列离子方程式的书写正确的是
| A.四氧化三铁和过量的稀硝酸反应:Fe3O4 + 8H+ =4H 2O + Fe 2+ + 2Fe 3+ |
| B.NaHCO3溶液与NaOH溶液反应: OH- + HCO3-= CO2↑+ H2O |
C.氯气溶于水Cl2+H2O 2H++Cl-+ClO- 2H++Cl-+ClO- |
| D.Ca(HCO3)2溶液与任意量澄清Ca(OH)2溶液反应:Ca2+ + HCO3 -+ OH-=CaCO3↓+H2O |
下列实验操作中,错误的是
| A.配制5%食盐溶液时,将称量的食盐放入烧杯中加适量的水搅拌溶解 |
| B.硫酸铜结晶水含量测定时,需用小火缓慢加热,防止晶体飞溅 |
| C.测定未知NaOH溶液浓度时,酸式滴定管需用标准酸液润洗2~3次 |
| D.配制0.1 mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 |
有硫酸镁溶液500ml,它的密度为1.20g/cm3,其中镁离子的质量分数为4.8%,则有关该溶液的说法不正确的是
| A.溶质的质量分数为24.0% |
| B.溶液的物质的量浓度为2.4mol/L |
| C.溶质和溶剂的物质的量之比为1:40 |
| D.硫酸根离子的质量分数为19.2% |
由CO、H2和O2组成的混合气体60 mL,在一定条件下恰好完全反应,测得生成物在101 kPa、120℃下对空气的相对密度为1.293,则原混合气体中H2所占的体积分数为
A.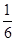 |
B. |
C.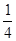 |
D. |
标准状况下,m g A气体和n g B气体的分子数相同。下列说法不正确的是
| A.同体积气体A和气体B的质量比为m∶n |
| B.25℃时,1 kg气体A和1 kg气体B的分子数之比为n∶m |
| C.同温同压下,气体A和气体B的密度之比为n∶m |
| D.标准状况下,等质量的气体A和气体B的体积之比为n∶m |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
| B.标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C.室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
| D.标准状况下,22.4 L甲醇中含有的氧原子数为1.0NA |