a根据氢氧化钙的溶解度曲线,完成下列问题。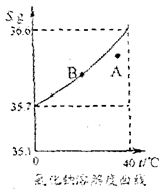
(1)曲线上满足A点指标的溶液在升高温度后会产生的现象是: ,此时的溶液中溶质质量分数将______ (选填“变大”或“变小”或“不变”)
(2)若向曲线上满足A点指标的溶液中加入生石灰,则溶液中的溶质质量奖
(选填“增加”或“减少”或“不变”)
b.根据氯化钠的溶解度曲线,完成下列问题。
(1)A点所示溶液为某温度下氯化钠的 (选填“饱和”或“不饱和”)溶液。
(2)将B点所示的溶液升高温度到40℃(忽略水的蒸发),此时溶液中溶质质量分数将
(选填“变大”或“变小”或“不变”)。
(3)B点代表20 ℃时氯化钠的溶解度为36.0g,若将满足B点指标的溶液恒温蒸发10g水,会有 g氯化钠晶体折出
用化学符号填空:
2 个氧原子 ;5 个硫化氢分子 ;
+2价的钡元素 ;硝酸亚铁 。
如图所示,两只U型管中分别加入纯净、等质量的铝粉和铁粉,同时将两端注射器内的液体(等质量、浓度为20%的稀硫酸)快速注入U型管中。
(1)写出铁粉与稀硫酸发生反应的化学方程式 。
(2)反应结束并冷却至室温,发现左端气球膨胀程度明显大于右端,若仅有一只U型管内的硫酸有剩余,则是 (填“左”或“右”)端的U型管。
(3)若将铝粉和稀硫酸换成其他两种化合物(或其溶液),也能观察到气球明显膨胀,这两种物质可能是(写化学式) 。
根据下图实验装置进行回答:
(1)写出标号仪器的名称① ②
(2)若要制取并收集一瓶氧气,用于做铁丝在氧气中的燃烧试验,则需 和配套。(在a~f中选择)
(3)在实验室制取并收集二氧化碳可选用 装置(填字母编号),写出实验室制取二氧化碳反应的化学方程式: 。验证二氧化碳收集满的方法是 。
(4)若将g装置装满水,用于收集氧气,则应将 (填“⑤”或“⑥”)与发生装置相连。
(5)以下是某研究小组探究影响反应速率部分因素的相关实验数据。
| 实验 序号 |
H2O2溶 液浓度% |
H2O2溶液体积/mL |
温度℃ |
MnO2的 用量/g |
收集氧气 的体积/mL |
反应所需 的时间/s |
| ① |
5 |
1 |
20 |
0.1 |
4 |
16.75 |
| ② |
15 |
1 |
20 |
0.1 |
4 |
6.04 |
| ③ |
30 |
5 |
35 |
2 |
49.21 |
|
| ④ |
30 |
5 |
55 |
2 |
10.76 |
通过实验①和②对比可知,化学反应速率与 有关;
铁是应用最广泛的金属.新型材料纳米级Fe粉能用作高效催化剂.实验室采用还原法制备纳米级Fe粉,其流程如图所示:
(1)纳米级Fe粉在空气中易自燃.实验中通入N2的目的是 。
(2)写出Ⅱ中H2还原FeCl2得到铁的化学方程式 ,该反应属于基本反应类型中的 反应。
如图是甲、乙两种物质的溶解度曲线,请结合图回答问题: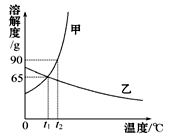
(1) ℃时,甲、乙两种物质的溶解度相等。
(2)溶解度随温度升高而降低的物质是 (填“甲”或“乙”)。
(3)可使甲物质从其饱和溶液中结晶析出的方法是 。
(4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数 乙溶液的溶质质量分数。(填“大于”“等于”或“小于”)。
(5)小明同学用甲物质进行以下实验: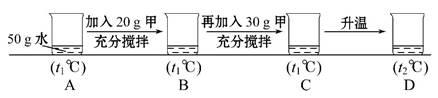
①实验过程中,B、C、D对应的溶液为不饱和溶液的是 。
②向B对应的溶液中再加入30 g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出。你认为“全部溶解”的原因是 。