碱金属钫(Fr)具有放射性,下列对其性质的预言中,错误的是
| A.在碱金属元素中它的原子核对最外层电子的引力最大 |
| B.钫在空气中燃烧时,只生成化学式为Fr2O的氧化物 |
| C.它的氢氧化物化学式为FrOH,是一种极强的碱 |
| D.它能跟水反应生成相应的碱和氢气,由于反应剧烈而发生爆炸 |
关于垃圾数字惊人:美国每年扔掉旧汽车900多万辆、各种纸2700多万吨、罐头盒480亿个。我国年消耗快餐盒16亿只,其中上海市日消耗量50万只……以下有关垃圾的说法不正确的是( )
| A.垃圾是污染物,一定条件下还可能继续反应产生二次污染 |
| B.垃圾处理要遵循无害化、减量化和资源化的原则 |
| C.废旧金属、玻璃等可回收利用,不属于垃圾 |
| D.没有绝对的垃圾,垃圾也可以回收利用 |
为实现中国在2000年消除碘缺乏病的目标,卫生部规定食盐必须加碘,其中的碘以碘酸钾(KIO3)形式存在。已知在溶液中IO3-可和I-发生反应:IO3-+5I-+6H+===3I2+3H2O,根据此反应,可用试纸和生活中常见的一些物质进行实验,证明在食盐中存在IO3-。进行上述实验时必须使用的物质是( )
①自来水 ②蓝色石蕊试纸 ③碘化钾淀粉试纸
④淀粉 ⑤食糖 ⑥食醋 ⑦白酒
| A.①③ | B.③⑥ |
| C.②④⑥ | D.①②④⑤⑦ |
对人体中的所需元素,下列四位同学的归纳整理完全正确的一组是( )
A.小芳认为,人体缺乏某些元素,会得不同疾病 |
B.小宝搜集资料发现,生活中人们常通过下列途径来补充人体必需的营养元素。如: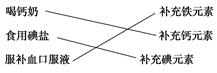 |
| C.小蓉为某些元素设计了一句广告词来反映其对人体的重要作用 碘——抗癌之星 硒——智力之星 氟——龋齿克星 |
| D.小红搜集资料发现,长期或大量摄入铝元素对人体的大脑和神经系统将造成损害,为此她提出下列建议: |

下列说法中不正确的是( )
| A.锌能提高脑神经的兴奋性 |
| B.钙能促进骨骼的生长发育 |
| C.缺铁能使人贫血 |
| D.缺氟能使人甲状腺肿大 |
下列属于强化营养型保健食品的是(双选)( )
| A.乳酸钙 | B.乳酸锌 |
| C.木糖醇 | D.深海鱼油 |