一定条件下将2mol SO2和2mol SO3气体混合于一固定容积的密闭容器中,发生反应:2SO2+O2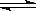 2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
2SO3,平衡时SO3为n mol,在相同温度下,分别按下列配比在上述容器中放入起始物质,平衡时SO3的物质的量可能大于n的是
| A.2 mol SO2+ 1 mol O2 |
| B.4 mol SO2+ 1 mol O2 |
| C.2 mol SO2+ 1 mol O2+ 2mol SO3 |
| D.3 mol SO2+0.5mol O2+ 1molSO3 |
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)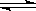 I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。
I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。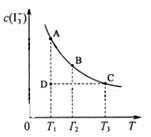
下列说法不正确的是
A.反应 I2(aq)+I-(aq)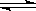 I3-(aq)的ΔH<0 I3-(aq)的ΔH<0 |
B.若反应进行到状态D时,一定有 |
| C.状态A与状态B相比,状态A的c(I2)大 |
D.若温度为 ,反应的平衡常数分别为K1、K2,则K1>K2 ,反应的平衡常数分别为K1、K2,则K1>K2 |
下列有关问题,与盐类的水解无关的是
| A.NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂 |
| B.盐酸可作铁制品的除锈剂 |
| C.实验室盛放Na2CO3溶液的试剂瓶不能用磨口玻璃塞 |
| D.加热蒸干AlCl3溶液得到Al(OH)3固体 |
在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) xC(g)+2D(g), 2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。则下列判断正确的是
xC(g)+2D(g), 2 min后该反应达到平衡,生成0.8 mol D,并测得C的浓度为0.2 mol·L-1。则下列判断正确的是
| A.x=2 |
| B.若混合气体的密度不变,则表明该反应达到平衡状态 |
| C.B的转化率为40% |
| D.2 min内A的反应速率为0.6 mol·L-1·min-1 |
醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
| A.升高温度,平衡正向移动,醋酸的电离常数Ka值增大 |
| B.0.10mol/L的CH3COOH溶液中加水稀释,溶液中c(OH-)增大 |
| C.CH3COOH溶液中加少量的CH3COONa固体,平衡逆向移动 |
| D.25℃时,欲使醋酸溶液的pH、电离常数Ka和电离程度都减小,可加入少量冰醋酸 |
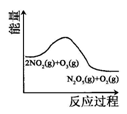
臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g) N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确
| A |
B |
C |
D |
 |
 |
 |
 |
| 升高温度,平衡常数减小 |
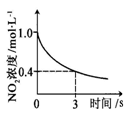
0~3s内,反应速率为:v(NO2)=0.2mol·L-1 |
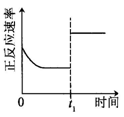
t1时仅加入催化剂,平衡正向移动 |
到达平衡时,仅改变x,则x为c(O2) |