某探究小组利用丙酮的溴代反应(CH3COCH3 + Br2 → CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。反应速率υ(Br2)通过测定溴的颜色消失所需的时间来确定。在一定温度下,获得如下实验数据:
| 实验序号 |
初始浓度c/mol·L-1 |
溴颜色消失 所需时间t/s |
||
| CH3COCH3 |
HC1 |
Br2 |
||
| ① ② ③ ④ |
0.80 1.60 0.80 0.80 |
0.20 0.20 0.40 0.20 |
0.0010 0.0010 0.0010 0.0020 |
290 145 145 580 |
分析实验数据所得出的结论不正确的是
| A.增大c(CH3COCH3),υ(Br2)增大 | B.实验②和③的υ(Br2)相等 |
| C.增大c(HCl),υ(Br2)增大 | D.增大c(Br2),υ(Br2)增大 |
已建立平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列叙述正确的是:(1)生成物的体积分数一定增加 (2)反应物的转化率一定增大
(3)生成物的产量一定增加 (4)反应物浓度一定降低
(5)正反应速率一定大于逆反应 (6)加入催化剂可以达到以上目的
| A.(1)(2) | B.(2)(5) | C.(3)(5) | D.(4)(6) |
 硫代硫酸钠溶液与稀硫酸反应的化学方程式:
硫代硫酸钠溶液与稀硫酸反应的化学方程式: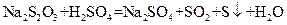 ,下列各组实验中最先出现浑浊的是
,下列各组实验中最先出现浑浊的是
| A.0.1mol/LNa2S2O3和H2SO4各5mL,加水5mL,反应温度10℃ |
| B.0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度10℃ |
| C.0.2mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
| D.0.1mol/LNa2S2O3和H2SO4各5mL,加水10mL,反应温度30℃ |
右图曲线a表示放热反应X(g)+Y(g)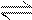 Z(g)+M(g)+N(s
Z(g)+M(g)+N(s ) 进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
) 进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是
| A.加催化剂 |
| B.加大X的投入量 |
| C.升高温度 |
| D.增大体积 |
反应4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率x
4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率x
A. (O2) =" 0.01mol·(L·s)" –1 B. (NO) =" 0.002mol·(L·s)" –1
C. (H2O) =" 0.006mol·(L·s)" –1 D . (NH3) =" 0.008mol·(L·s)" –1
. (NH3) =" 0.008mol·(L·s)" –1
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速度,且不影响生成氢气的总量,可向盐酸中加入适量的
| A.NaNO3 (溶液) | B.KCl(溶液) | C.NaCl(固体) | D.NaOH (固体) |