某温度时,BaSO4在水中的沉淀溶解平衡:BaSO4(s) 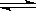 Ba2+(aq)+SO(aq) Ksp=c(Ba2+)·c(SO ),沉淀溶解平衡曲线如图所示。 下列说法正确的是
Ba2+(aq)+SO(aq) Ksp=c(Ba2+)·c(SO ),沉淀溶解平衡曲线如图所示。 下列说法正确的是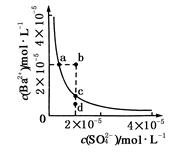
| A.b点时c(Ba2+)·c(SO )小于Ksp |
| B.a点对应的Ksp等于c点对应的Ksp |
| C.加水稀释可以使溶液由b点变到c点 |
| D.加入适量的Na2SO4可以使溶液由a点变到c点 |
现有四种元素的基态原子的电子排布式如下:
①1s22s22p63s23p4②1s22s22p63s23p3③1s22s22p3④1s22s22p5
则下列有关比较中正确的是( )
| A.第一电离能:④>③>②>① |
| B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① |
| D.最高正化合价:④>③=②>① |
下列说法正确的是( )
| A.因为p轨道是“8”字形的,所以p电子走“8”字形 |
| B.第三电子层,有3s、3p、3d三个轨道 |
| C.氢原子中只有1个电子,故氢原子只有一个轨道 |
| D.原子轨道与电子云都是用来形象描述电子运动状态的 |
外围电子排布式为3d104s1的元素在周期表中应位于( )
| A.第四周期ⅠB族 | B.第五周期ⅡB族 |
| C.第四周期ⅦB族 | D.第五周期ⅢB族 |
下列有关表述正确的是( )
| A.硫离子的电子排布式:1s22s22p63s23p4 |
B.H2O的电子式: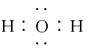 |
C.N原子最外层电子的轨道表示式: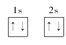  |
D.K的原子结构示意图: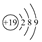 |
在d轨道中电子排布成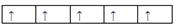 ,而不排成
,而不排成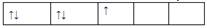 最直接的根据是 ( )
最直接的根据是 ( )
| A.能量最低原理 | B.泡利不相容原理 |
| C.洪特规则的特例 | D.洪特规则 |