下列各组中的离子能在pH=1的无色溶液中大量共存的是
| A.Ba2+、Na+、I-、ClO- | B.Mg2+、Cl-、Al3+、NO3- |
| C.K+、Fe2+、Cl-、MnO4- | D.Ca2+、Na+、Fe3+、Br- |
下列事实,不能用勒夏特列原理解释的是()
A.溴水中有平衡:Br2+H2O  HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 HBr+ HBrO 加入 AgNO3溶液后,溶液颜色变浅 |
B.对CO(g) + NO2 (g) CO2 (g)+ NO(g) 平衡体系增大压强可使颜色变深 CO2 (g)+ NO(g) 平衡体系增大压强可使颜色变深 |
| C.高压比常压有利于合成SO3的反应 |
| D.合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施 |
某新型可充电电池,能长时间保持稳定的放电电压,该电池的总反应为:
则以下说法不正确的是:


| A.放电时负极反应为:Zn-2e–+2OH–=Zn(OH)2 |
| B.放电时正极反应为:FeO42–+4H2O+3e–=Fe(OH)3+5OH– |
| C.充电时阳极附近溶液的碱性减弱 |
| D.放电时每转移3 mol电子,正极有1 molK2FeO4被氧化 |
下列说法或表示方法正确的()
A.已知C(s)+O2(g)===CO2(g)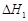 ;C(s)+ ;C(s)+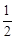 O2(g)===CO (g) O2(g)===CO (g)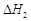 ,则 ,则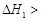 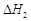 |
B.在稀溶液中,H+(aq)+OH-(aq)===H2O(l) 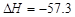 kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3 kJ kJ·mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热大于57.3 kJ |
C.由C(石墨)===C(金刚石);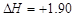 kJ·mol-1可知,金刚石比石墨稳定 kJ·mol-1可知,金刚石比石墨稳定 |
| D.已知氢气的标准燃烧热为-285.8 kJ·mol-1,相应的热化学方程式为2H2(g) + O2(g)=2H2O(l) ΔH = –285.8kJ·mol-1 |
观察下列几个装置示意图,有关叙述正确的是 ( )
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源正极相连 |
| C.装置③中外电路电子由a极流向b极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
用石墨作电极,电解1 mol/L下列物质的溶液,溶液的pH保持不变的是()
| A.HCl | B.NaOH | C. NaCl | D.Na2SO4 |