下列各组元素均属于p区元素的是
| A.H、He、N | B.O、S、P | C.Fe、Ar、Cl | D.Na、Li、Mg |
分别在PH=1的酸溶液和PH=14的NaOH溶液中加入足量的铝,放出氢气的量前者多,其原因可能是:①两溶液的体积相同,而酸是多元强酸;②两溶液的体积相同,酸是弱酸;③酸溶液的体积比NaOH溶液体积大;④酸是强酸,且酸溶液的浓度比NaOH溶液浓度大;其中正确的为
| A.只有②和③ | B.只有②和④ | C.只有①和③ | D.只有① |
用标准盐酸滴定未知浓度的NaOH溶液时,下列操作能引起偏低误差的是
| A.锥形瓶用待测液润洗2~3次 |
| B.指示剂变色后又立即就停止滴定 |
| C.滴定前酸式滴定管俯视读数,滴定后又仰视 |
| D.滴定结束后,酸式滴定管尖嘴处悬挂一滴液体 |
下列说法正确的是
| A.向0.1 mol·L-1 KNO3溶液中滴加稀盐酸使溶液的pH=5,此时混合液中c(K+)<c(NO3-) |
| B.25 ℃时,0.1 mol·L-1氨水和0.05 mol·L-1氨水中c(OH-)之比是2∶1 |
| C.0.1 mol·L-1NH4Cl溶液中c(Cl-)=c(NH4+) |
| D.向CH3COONa溶液中加入适量CH3COOH使混合液pH=7,此时溶液中c(Na+) =c(CH3COO-) |
在一定温度下,向a L密闭容器中加入1molX气体和2 molY气体,发生如下反应:X(g) + 2Y(g) 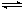 2Z(g)此反应达到平衡的标志是
2Z(g)此反应达到平衡的标志是
| A.容器内压强不随时间变化 |
| B.容器内各物质的浓度完全相同 |
| C.容器内X、Y、Z的浓度之比为1∶2∶2 |
| D.单位时间消耗0.1molX同时生成0.2molZ |
下列说法正确的是
| A.甲基橙的变色PH范围在4.4~6.2之间。 |
| B.保护海轮外壳以及石油管道通常是用牺牲阳极的阴极保护法。 |
| C.电离常数可以表示弱酸的相对强弱,电离常数越小,弱酸的酸性越强。 |
| D.弱电解质的电离是一个放热过程。 |