已知Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl 组成的固体混合物。向其中逐渐滴加溶质质量分数为10%的稀盐酸。放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
(1) 当滴加稀盐酸至图中B点时,烧杯中溶液的
pH 7(填>、=、<)。
(2) 原混合物中碳酸钠的质量。
(3) 当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常
温),通过计算求出其中溶质的质量分数。(计算结果保留一位小数)。
将12.5g石灰石与足量稀盐酸充分反应,产生的二氧化碳的质量与时间关系如图所示(杂质不和盐酸反应,也不溶解)。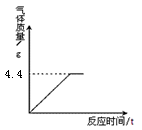
计算:①石灰石中所含碳酸钙的物质的量(根据化学方程式列式计算)。(15)
②石灰石中碳酸钙的质量分数为(16)。
为了测定某石灰石中碳酸钙的含量,现取12克石灰石放入烧杯中,向其中加入70克稀盐酸,两者恰好完全反应(杂质不与酸反应,反应中水分蒸发忽略),测得烧杯中的剩余物的质量为78.7克。试计算:
①生成二氧化碳的物质的量是⑴摩尔。
②该石灰石中碳酸钙的纯度为⑵。(根据化学方程式列式计算)
完成下列研究性学习的有关内容;探究氯酸钾和二氧化锰混合物中二氧化锰的质量分数。(计算结果保留到0.01%)
[研究方案]先称取一定质量的氯酸钾和二氧化锰混合物,放入大试管中加热至质量不再变化为止。根据质量守恒定律,固体物质减轻的质量即为产生氧气的质量,从而求出氯酸钾的质量。(学习小组同学事先查阅资料获知,二氧化锰的质量在反应前后不变且在水中难溶)
(1)[解决问题]实验测得固体混合物质量随加热时间变化的相关数据如图所示。请你完成下列问题: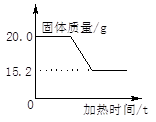
①反应后生成氧气的质量是;
②原混合物中氯酸钾的质量是;
③原混合物中二氧化锰的质量分数是。
(2)[继续研究]为了分离回收二氧化锰和氯化钾,他们在反应后的固体混合物中加入92.55g水使其中的氯化钾完全溶解,然后过滤使二氧化锰与溶液分离。请你计算他们得到的滤液中氯化钾的质量分数。(过滤中水的损失不计)。
化学小组同学欲测定铜锌合金中铜元素的质量分数。
(1)甲方案:取10 g合金粉末,加入少量稀硫酸后,收集到0.1 g氢气,计算合金中铜元素的质量分数为67.5%。老师指出其测定结果不准确,原因是。
(2)乙方案:取10 g合金粉末,加入足量硫酸铜溶液,充分反应后,过滤,洗涤,烘干,测得固体质量为9.9 g。计算合金中铜元素的质量分数。(写出计算过程)
某化学探究小组的同学为测定某样品中铁的质量分数,他们将样品放入烧杯中,再加入足量的稀盐酸,至不再有气泡产生为止.各步称量数据如下:(稀盐酸的挥发可忽略不计)
生铁样品质量为11.5 g ;烧杯的质量 为32.5 g;所加稀盐酸的质量为200.0 g;
反应后烧杯及所盛物质的总质量为243.6 g 请回答下列问题:
(1)反应中产生气体的质量是g.
(2)计算该生铁样品中铁的质量分数(写出计算步骤,计算结果精确到0.1%).