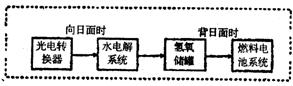
I.我国即将建成自己的载人空间站。载人航天器的生态系统中,不仅要求分离去除CO2,还要求提供充足的O2。
⑴某种电化学装置可实现如下转化:2CO2=2CO+O2,CO可用作燃料。已知该反应的某极反应为:4OH--4e-=O2↑+2H2O,则另一极反应为: 。
⑵有人提出,可以设计某温度下的反应:2CO=2C+O2(△H>O、△S<O)来消除CO的污染。请你判断该温度下上述反应是否能发生并说明理由是 。
Ⅱ.大气固氮属于自然固氮,合成氨是目前人工固氮的主要方法。科学家一直致力“人工固氮”新方法的研究。
⑴有关大气固氮(以N2+O2 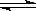 2NO为例)、人工固氮(以N2+3H2
2NO为例)、人工固氮(以N2+3H2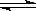 2NH3为例)反应的平衡常数
2NH3为例)反应的平衡常数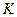 的值如下表。
的值如下表。
| 反应 |
N2+02 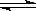 2NO 2NO |
N2+3H2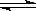 2NH3 2NH3 |
||
| 温度/℃ |
27 |
2000 |
100 |
400 |
| K |
3.84×10-31 |
0.1 |
3.4×109 |
2.0x104 |
下列说法正确的是 。(填字母)
a.大气固氮与人工固氮都是放热反应
b.人类模拟大气固氮无现实意义
c.寻找在常温下合成氨的高效催化剂是目前人工固氮的新方向
d.在常温下,人工固氮非常容易进行
⑵已知:N2(g)+3H2(g) 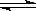 2NH3(g)
2NH3(g) 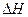 =-92.4kJ·mol-1
=-92.4kJ·mol-1
2H2(g)+02(g)="2H20(1) " 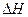 ="-571.6" kJ·mol-1
="-571.6" kJ·mol-1
据报道,在常温、常压、光照、催化剂的条件下,N2可以与水反应,则反应 N2(g)+3H20(1)=2NH3(g)+3/2O2(g)的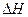 = KJ·mol-1。
= KJ·mol-1。
⑶某研究小组在673 K、30 MPa下,在体积为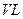 的密闭容器中进行反应:N2(g)+3H2(g)
的密闭容器中进行反应:N2(g)+3H2(g) 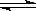 2NH3(g),其
2NH3(g),其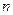 (H2)和
(H2)和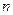 (NH3)随时间变化的关系如图所示。
(NH3)随时间变化的关系如图所示。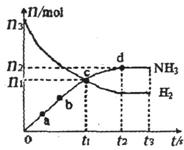
①下列叙述正确的是 。(填字母)
A.点a的正反应速率比点b的大
B.点c处反应达到化学平衡状态
C.若t3时由673 K升至773 K,则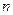 (H2)将增大
(H2)将增大
②从开始到平衡时反应的平均速率(以H2的浓度变化表示)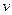 (H2)= 。
(H2)= 。
③若开始时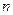 (N2)=
(N2)=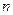 (H2),则反应的平衡常数
(H2),则反应的平衡常数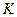 = (用代数式表示)。
= (用代数式表示)。
25℃时,50mL0.1mol/L醋酸中存在下述平衡:_______________________。若分别作如下改变,对上述平衡有何影响?
⑴加入少量冰醋酸,平衡将__________,溶液中c(H+)将__________(增大、减小、不变);
⑵加入一定量蒸馏水,平衡将__________,溶液中c(H+)将__________(增大、减小、不变)
⑶加入少量0.1mol/L盐酸,平衡将__________,溶液中c(H+)将__________(增大、减小、不变)
⑷加入20mL0.10mol/LNaCl,平衡将__________,溶液中c(H+)将__________(增大、减小、不变)
氢化阿托醛 是一种重要的化工原料,其合成路线如下:
是一种重要的化工原料,其合成路线如下: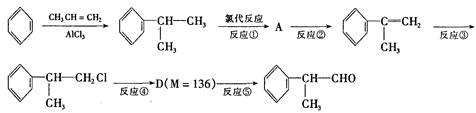
(1)在合成路线上②③的反应类型分别为② ③ 。
(2)反应④发生的条件是。
今有相对分子质量为M的有机物,燃烧后只生成二氧化碳和水。
①若有机物是M=72的烃,请写出所有可能的结构简式:_________;_________;_________。
②若M=58,且1mol该有机物与足量的银氨溶液作用,可析出4molAg, 则其结构简式为:_________________
则其结构简式为:_________________
③若A是分子 式为C12H16的烃,B是含4个氧原子的烃的含氧衍生物,A、B相对分子质量相等,则B的分子式可能为:______________________。
式为C12H16的烃,B是含4个氧原子的烃的含氧衍生物,A、B相对分子质量相等,则B的分子式可能为:______________________。
中国食疗网发布“反式脂肪酸预警报告”,报告称:脂肪酸分为顺式脂肪酸、反式脂肪酸两种,摄入过多的反式脂肪酸,容易堵塞血管而导致心脑血管疾病。两种脂肪酸的结构如图所示。试回答下列问题:
(1)脂肪酸中所含官能团的名称是_______________________________。
(2)上述“A”、“B”结构能表示“反式脂肪酸”的是(填“A”或“B”)
(3)上述顺(反)式脂肪酸都能与H2在一定条件下发生氢化反应,其产物关系为 。
。
| A.同分异构体 | B.同系物 | C.同一种物质 | D.对映异构体 |
(4)CH2 =CHCH2OH发生加成聚合反应后,所得产物的结构简式为______________
=CHCH2OH发生加成聚合反应后,所得产物的结构简式为______________
现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子 Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl-、OH-、NO3-、CO32-、X中的一种。
(1)某同学通过分析,认为无需 检验就可判断其中必有的两种物质是和(填化学式)。
检验就可判断其中必有的两种物质是和(填化学式)。
(2)为了确定X,现将(1)中的两种物质记为A和B,含X的物质记C,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时也产生红褐色沉淀,向该沉淀中滴人稀硝酸沉淀部分溶解,最后留有白色沉淀不再溶解。则X为。
A.SO32-B.SO42-C.CH3COO- D.SiO32-
(3)B的水溶液显性,原因为。(用离子方程式表示)
(4)将0.02 molA与0.0 1molC同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的物质的量为 (保留一位小数)
(保留一位小数)
(5)将Cu投人到装有D溶液的试管中,Cu不溶解;再 滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的
滴加稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现。则物质D一定含有上述离子中的 (填相应的离子符号)。有关反应的离
(填相应的离子符号)。有关反应的离 子方程式为:。
子方程式为:。
(6)利用上述已经确定的物质,可以检验出D、E中的阳离子。请简述实验操作步骤、现象及结论。