对于下列事实的解释错误的是
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
B.浓硫酸能与铜反应,说明硫酸具有强氧化性 |
| C.氯气使潮湿的红色纸褪色,说明氯气有漂白性 | |
| D.浓盐酸与MnO2能反应生成氯气,说明浓盐酸具有还原性和酸性 |
R、X、Y、M、Z 5种短周期主族元素的原子半径依次减小,X、Y、Z的电子层数之和为5,X元素原子的最外层电子数是它的电子层数的2倍,Y元素原子的最外层电子数是X和Z两元素原子最外层电子数的总和,M是地壳中含量最多的元素,R与Z的最外层电子数相同。下列叙述正确的是( )
| A.Z与M形成的化合物中不可能含有非极性键 |
| B.对应氢化物的热稳定性:X > Y >M |
| C.单质的还原性:R> M>Y>X |
| D.X、Y、M、Z 4种元素组成的离子化合物受热易分解 |
下表是元素周期表的一部分,有关说法正确的是( )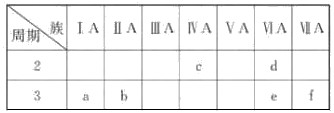
| A.e的氢化物比d的氢化物稳定 |
| B.a、b、e三种元素的原子半径:e>b>a |
| C.6种元素中,c元素单质的化学性质最活泼 |
| D.c、e、f的最高价氧化物对应的水化物的酸性依次增强 |
甲、乙、丙、丁是原子序数依次增大的4种短周期元素,A、B、C、D、E是由其中的2种或3种元素组成的化合物,F是由丙元素形成的单质。已知:A+B=D+F,A+C=E+F; 0.1 mol·L-1D溶液的pH为13(25 ℃)。下列说法正确的是( )
A.原子半径:丁>丙>乙>甲
B.乙元素在周期表中的位置为第三周期第ⅣA族
C.1 mol A与足量B完全反应共转移了1 mol电子
D.1.0 L 0.1 mol·L-1E溶液中阴离子总的物质的量小于0.1 mol
X、Y、Z、W、Q是原子序数依次增大的5种短周期主族元素。其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示。下列说法正确的是( )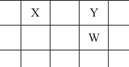
| A.5种元素中,原子半径最大的是W |
| B.Y与Z形成的化合物都可以和盐酸反应 |
| C.Y的简单阴离子比W的简单阴离子还原性强 |
| D.Z与Q形成的化合物水溶液一定显酸性 |
正长石的主要成分为硅酸盐,由前20号元素中的4种组成,化学式为XYZ3W8。其中,只有W显负价。X、Y的最外层电子数之和与Z的最高正价数相等。Y3+与W的阴离子具有相同的电子层结构。X、W的质子数之和等于Y、Z的质子数之和。下列说法错误的是( )
| A.X的离子半径>Y的离子半径 |
| B.Z的氢化物的稳定性<W的氢化物的稳定性 |
| C.Y的氧化物既能与盐酸反应,又能与NaOH溶液反应 |
| D.X2W2、Y2W3两种化合物含有的化学键类型完全相同 |