下列叙述中,不正确的是
| A.含有离子键的化合物一定是离子化合物 |
| B.单质中不一定存在非极性键 |
| C.非金属原子之间只能构成共价化合物 |
| D.Cl2的沸点比F2高,这与分子间作用力的大小有关 |
如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是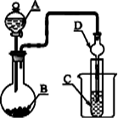
| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B.若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色 |
| C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀又溶解 |
| D.若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊 |
将足量的CO2不断通入NaOH、Ba(OH)2、NaAlO2的混合溶液中,生成沉淀与通入CO2的量的关系可表示为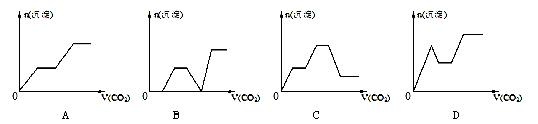
向Fe2O3、CuO、Fe、Cu的混和粉末中加入过量的稀硫酸,充分反应后,仍有红色粉末存在,则关于所得溶液中阳离子的判断正确的是
| A.一定有Fe2+,可能有Cu2+ | B.一定有Fe2+、Cu2+,可能有Fe3+ |
| C.只有Fe2+和Cu2+ | D.只有Fe2+ |
向一定量的FeO、Fe、Fe2O3的混合物中加入100mL 1mol/L的盐酸,恰好使混合物完全溶解,放出224 mL标况下的气体,所在得溶液中滴入硫氰化钾溶液无血红色出现(即无3价铁)。若用足量CO在高温下还原同质量的此混合物,能得到铁的质量是
| A.11.2g | B.5.6g | C.2.8g | D.无法计算 |
同温同压下,在3支体积不同的试管中分别充满等体积混合的2种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中溶质的物质的量浓度分别为c1、c2、c3(假设溶质全在试管中),则下列关系正确的是
| A.c1>c2>c3 | B.c1>c3>c2 | C.c1=c3>c2 | D.c1=c2>c3 |