分别处于第二、三周期的主族元素A和B,它们离子的电子层相差两层,已知A处于第m族,B处于第n族,A只有正化合价,则A、B原子核外的电子总数分别为
A.m+2、10+n B.m、n
C.3、7 D.m-2、10-n
设NA为阿伏加德罗常数的值,下列叙述正确的是
| A.标准状况下,2.24L苯中含0.6NA个氢原子 |
| B.22.4LCl2通入水中充分反应,共转移NA个电子 |
| C.1L1mol·L-1氯化铜溶液中Cu2+的数目小于NA |
| D.0.1mol铁在0.1molCl2中充分燃烧,转移的电子数为0.3NA |
下列说法不正确的是
| A.热水瓶胆中的水垢可以用食醋除去 |
| B.可以用淀粉溶液检验加碘盐中是否含碘元素 |
| C.在蔗糖中加入浓硫酸出现黑色物质,说明浓硫酸具有脱水性 |
| D.做红烧鱼时,常加一些食醋和酒会更香,是因为生成少量的酯 |
在一恒定的容器中充入2 mol X和1 mol Y发生反应:2X(g)+Y(g) nZ(g)达到平衡后,Z的体积分数为a%;若维持容器的容积和温度不变,按起始物质的量X为0.6 mol,Y为0.3 mol,Z为1.4 mol充入容器中,达到平衡后,Z的体积分数仍为a%,则n的值为( )
nZ(g)达到平衡后,Z的体积分数为a%;若维持容器的容积和温度不变,按起始物质的量X为0.6 mol,Y为0.3 mol,Z为1.4 mol充入容器中,达到平衡后,Z的体积分数仍为a%,则n的值为( )
| A.可能为2,也可能为3 | B.只能为3 |
| C.只能为2 | D.无法确定 |
下列各装置中,在铜电极上不能产生气泡的是( )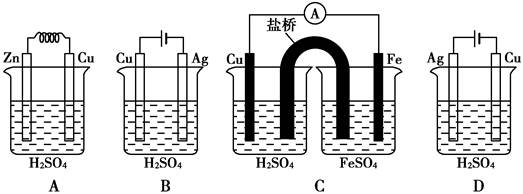
关于下图电化学装置中的电极名称、材料及反应均可能正确的是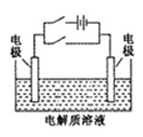
| A.阴极(Cu片)2C1――2e-=Cl2↑ |
| B.正极(石墨棒):Fe3+ +e-= Fe2+ |
| C.阳极(Cu片):4OH――4e-=2H2O+O2↑ |
| D.负极(Fe钉):Fe-3e-=Fe3+ |