(6分,每空2分)已知有1H216O、D2S、3H218O、S17O2、2H2S、S16O2,其中有__ __种元素, 种核素, 种分子。
W、X、Y、Z是短周期主族元素,它们的核电荷数依次增大。下表列出它们的性质和原子结构:
| 元素编号 |
元 素性质或原子结构 素性质或原子结构 |
| W |
原子电子层数与核外电子数相等 |
| X |
核外s能级上的电子总数与p能级上的电子总数相 等 等 |
| Y |
元素的原子半径在该周期中最大(除稀有气体外) |
| Z |
原子核外p能级上的电子总数比s能级上的电子总数多2 |
(1)元素符号:X_______________,Z________________。
(2)Y元素原子的核外电子排布式为__________________。
(3)X元素原子的核外有种不同形状的电子云。
(4)Y元素的单质在W和X形成的化合物中反应的离子方程式为
___________________________________________________________________ 。
在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) |
0 |
1 |
2 |
3 |
4 |
5 |
| n(NO)/mol |
0.020 |
0.010 |
0.008 |
0.007 |
0.007 |
0.007 |
(1)写出该反应的平衡常数表达式:K=__________________________。
已知:K(300℃)>K(350℃),该反应是__________热反应(填“放”或“吸”)。
(2)上述反应达平衡时,NO的转化率=__________________。
(3)下图中表示NO2的变化的曲线是____________(选填字母,下同)。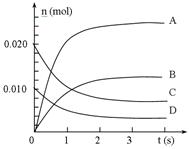
(4)能说明该反应已经达到平衡状态的是___________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=2v正(O2) D.NO和NO2两物质的浓度相等
(5)为使该反应的反应速率增大,且平衡向正反应方向移动的是__________。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度 D.选择高效的催化剂
固定和利用CO2能有效地利用资源,并减少空气中的温室气体.CO2与化合物A反应生成化合物B,如下反应式(其它试剂、产物及反应条件均省 略)。
略)。
(1)化合物B的分子式为__________,1 mol该物质完全燃烧需消耗_________mol O2。
(2)由 通过消去反应制备A的化学方程式为(注明反应条件):
通过消去反应制备A的化学方程式为(注明反应条件):
_______________________________________________________________________。
(3)B与过量C2H5OH在酸催化下发生酯化反应,生成的有机物的结构简式为:
__________________________________________。
(4)与CO2类似,CO也能被固定和利用。在一定条件下,CO、 和
和
H2三者发生反应(苯 环不参与反应),生成化合物C的分子式为C9H8O,且物质C能发生银镜反应。写出生成物C可能的结构简式:
环不参与反应),生成化合物C的分子式为C9H8O,且物质C能发生银镜反应。写出生成物C可能的结构简式:
___________________________________________________________________。
有机物A的结构简式为 ,该有机物A可通过不同化学反应分别制得下列B、C、D和E四种物质。
,该有机物A可通过不同化学反应分别制得下列B、C、D和E四种物质。
请回答下列问题:
(1)指出反应的类型:A → C。
(2)在A~E五种物质中,互为同分异构体的是(填代号)。
(3)写出由A生成B的化学方程式
。
(4)物质D结构中含有苯环、___________________________________等官能团。
(5)C能形成高聚物,该高聚物的结构简式为。
(6)写出D与NaOH溶液共热反应的化学方程式
。
将Al2O3和Fe2O3的混合物进行如下实验,试写出各步操作所发生反应的离子方程式:
①将混合粉末用硫酸充分溶解:
②在溶液中用过量浓氨水中和,得到沉淀:
③在沉 淀中滴加KOH溶液,充分反应滤出沉淀得:
淀中滴加KOH溶液,充分反应滤出沉淀得:
④往滤液中通入足量CO2:。