下表列出了除去物质中所含少量杂质的方法,其中错误的是
| |
物质 |
所含杂质 |
除去杂质的方法 |
| A |
CO |
CO2 |
通过足量氢氧化钠溶液,干燥 |
| B |
NaCl |
泥沙 |
溶解、过滤、蒸发 |
| C |
NaOH溶液 |
Na2CO3 |
加入足量稀盐酸至不再产生气泡 |
| D |
Cu(NO3)2溶液 |
AgNO3 |
加入过量的铜粉,过滤 |
下列化学用语中,书写正确的是()
| A.2个氢离子H2+ | B.氧化铁FeO |
| C.五氧化二磷P2O5 | D.硝酸铝A1NO3 |
2008年“5. 12汶川大地震”抗震救灾现场,疾病预防控制中心的防疫人员在大街小巷喷洒“含氯消毒液”。“含氯消毒液”中的“氯”在这里指的是()
| A.单质 | B.元素 | C.离子 | D.分子 |
关于下列粒子结构示意图的说法不正确的是()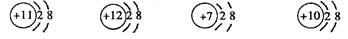
| A.它们均为稀有气体 | B.它们的核外电子排布相同 |
| C.它们都有相对稳定结构 | D.它们核外都有2个电子层 |
常温下碳的化学性质不活泼,这主要取决于碳原子的()
| A.核电荷数 | B.最外层电子数 | C.核内中子数 | D.核外电子数 |
下列仪器中,能在酒精灯火焰上直接加热的是()
| A.试管 | B.量筒 | C.烧杯 | D.集气瓶 |