某课外兴趣小组的同学向Na2SiO3溶液中滴加盐酸,预计会生成H2SiO3胶体,用激光笔照射会出现“丁达尔现象”。但令人意想不到的是,试管中在出现硅酸胶体的同时也出现了大量气泡,为什么会出现这种现象呢?甲乙两同学进行了大胆的推测。
甲同学推测是生成了硅酸胶体,造成HCl在溶液中的溶解度变小,最终从溶液中逸出;
乙同学咨询了实验员得知这瓶Na2SiO3溶液已经放置很长一段时间,他推测溶液可能已经变质,故导致以上现象的出现。
(1)请设计一个最简单的实验验证甲同学的推测是否正确: ;
(2)乙同学取这瓶久置的硅酸钠溶液,用激光笔照射,发现有光柱出现,说明在这瓶硅酸钠溶液中已经有 胶体生成。推测产生的气体可能是 ,然后乙同学又做了两个实验进行验证:
I取少量该瓶溶液,向其中滴加 ,并检验产生的气体。请写出检验该气体的常用方法: ;
II取硅酸钠固体,配成饱和溶液,现配现用,滴入盐酸,观察现象;
通过以上实验,证明了乙同学观点,请写出所对应的化学反应方程式:
、 ;
该小组同学还发现按教材所述的操作方法和条件制备硅酸胶体,有时需要很长时间才能使溶胶慢慢凝聚,甚至不易形成凝胶,效果很不理想。因此,该组同学又对实验条件和操作进行探究,相关实验数据如下表:
| |
硅酸钠溶液浓度 |
盐酸浓度 |
试剂加入顺序 |
出现凝胶时间(s) |
| 实验1 |
饱和溶液 |
1:2(盐酸和水体积比,下同) |
将Na2SiO3溶液滴加到稀盐酸中 |
21 |
| 实验2 |
稀溶液(1体积饱和溶液和3体积水混合) |
1:2 |
将稀盐酸滴加到Na2SiO3溶液中 |
38 |
| 实验3 |
饱和溶液 |
1:4 |
将Na2SiO3溶液滴加到稀盐酸中 |
10 |
| 实验4 |
稀溶液(1体积饱和溶液和3体积水混合) |
1:4 |
将稀盐酸滴加到Na2SiO3溶液中 |
50 |
该组部分同学通过实验得出结论:使用饱和Na2SiO3溶液和稀盐酸,将Na2SiO3溶液滴加到稀盐酸中效果较好。但该组另外一部分同学认为基于限定的条件,该探究实验设计组数不够,不能保证结论的准确性,要使实验具有说服力至少要做组实验。
某同学设计如下实验验证炭与浓硫酸的反应产物及产物的某些性质。
(1)装置A中盛放浓硫酸的仪器名称是。
(2)若要证明有水生成,需要在A、B之间加装盛有的干燥管。
(3)利用装置B可以完成的实验是。
(4)若在E中盛装澄清石灰水,C中盛装酸性高锰酸钾溶液,则D中的试剂是,其作用是;写出C中关于高锰酸钾发生反应的离子方程式。
(4分)利用下图所示装置制备氧气并进行相关实验探究。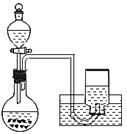
(1)将3.9g过氧化钠放入烧瓶中,加入100mLH2O,用排水法收集气体,过氧化钠与水反应的化学方程式是。
(2)已知:酚酞在c(OH-) 为1.0×10-4mol/L~2.5mol/L时呈红色,且半分钟内不褪色;H2O2具有氧化性和漂白性,在MnO2催化条件下迅速分解。取上述实验得到的溶液于试管中,滴入2滴酚酞试液,溶液变红色,片刻红色褪去。假设实验中液体体积不变,回答下列问题(任答一问):
①甲同学认为“红色迅速褪去”是由于溶液中c(OH-)过大造成的。请用计算结果说明上述观点是否正确。答:。 ②乙同学认为“红色迅速褪去”是由于溶液中存在H2O2,其来源可能是Na2O2+2H2O=2NaOH+H2O2。简述你设计简单实验证明烧瓶内溶液中含H2O2的实验原理。
②乙同学认为“红色迅速褪去”是由于溶液中存在H2O2,其来源可能是Na2O2+2H2O=2NaOH+H2O2。简述你设计简单实验证明烧瓶内溶液中含H2O2的实验原理。
答:。
用0.2000mol/L NaOH溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
(A)移取15.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准NaOH溶液润洗碱式滴定管2-3次
(C)把盛有标准溶液的滴定管固定好,使滴定管尖嘴充满溶液
(D)取标准溶液注入滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管下面,用标准NaOH溶液滴定至终点,记下滴定管液面的刻度
完成以下各空:
(1)正确操作的顺序是B→_____→_____→_____→A→F;
(2)三次滴定消耗NaOH溶液的体积如下:
| 实验序号 |
1 |
2 |
3 |
| 消耗NaOH溶液的体积(mL) |
20.05 |
20.00 |
19.95 |
则该盐酸溶液的准确浓度为_____________ mol/L。(保留小数点后4位)
(3)用标准的NaOH溶液滴定未知浓度的盐酸,下列情况可能造成测定结果偏高的是:。
A.配制标准溶液时称量的氢氧化钠固体中混有Na2CO3杂质
B.滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C.盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗
D.滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
(14分)用密度为1.84g/mL,质量分数为98%的浓硫酸配制100 ml 3.0mol/L 稀硫酸的实验步骤如下:①计算所用浓硫酸的体积②量取一定体积的浓硫酸③稀释④转移
⑤洗涤⑥定容⑦摇匀
(1)所需浓硫酸的体积是。
(2)第③步实验的操作是。
(3)第⑥步实验的操作是。
(4)下列情况对所配制的稀硫酸浓度有何影响?(用字母填写a.偏大 b.偏小 c.无影响)
| A.所用的浓硫酸长时间放置在密封不好的容器中 |
| B.容量瓶用蒸馏洗涤后残留有少量的水 |
| C.所用过的烧杯、玻璃棒未洗涤 |
| D.量取浓硫酸时仰视量筒上的刻度取用浓硫酸 |
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
F.把配好的溶液倒入用蒸馏水洗净而未干的试剂瓶中备用
(5)本实验最浪费时间的地方是将稀释后的硫酸冷却至室温,为了节约时间,简单易行的加
快稀硫酸冷却的方法是_______________________________________.
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 ="=" 2Na2CO3 + O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
(1)A中制取CO2 的装置,应从下列图①和②中选哪个图:
B装置的作用是,C装置内出现的现象是。为了检验E中收集到的气体,在取出集气瓶后,用的木条伸入集气瓶内,木条会出现。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因:。
(3)反应完毕时,若测得E中的集气瓶收集到的气体250毫升,又知氧气的密度为1.43克/升,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值(偏大或偏小),相差约毫升(取整数值,所用数据均在标准状况下测定),这可能是由于。
(4)你认为上述A---E的实验装置中,E部分是否安全、合理?
E是否需要改进,若需要改进,应改为下图中的(填甲、乙、丙、丁).