对于常温下pH为1的硝酸溶液, 下列叙述正确的是
下列叙述正确的是
A.该溶液lmL稀释至100mL后,pH等于3 |
B.向pH为1的硝酸溶液中加入等体积、pH为13的氨水恰 好完全中和 好完全中和 |
C.该溶液中硝酸电离出的c(H+)与水电离出的c(H+)之比值为1×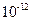 。 。 |
D.该溶液中水电离出的c(H+)是pH为3的硝酸中水电离出的c(H+)的100倍 |
工业通过氨的催化氧化制取硝酸,其中一个反应3NO2(g) + H2O(l) 2HNO3(aq) + NO(g)ΔH < 0,现欲提高反应物NO2的转化率,增加硝酸的产量,下列采取的措施可行的是
2HNO3(aq) + NO(g)ΔH < 0,现欲提高反应物NO2的转化率,增加硝酸的产量,下列采取的措施可行的是
| A.增加压强 | B.加大水量 | C.升高温度 | D.加入催化剂 |
对一已经达到化学平衡的体系,下列说法正确的是
| A.化学反应速率变化时,化学平衡一定发生移动 |
| B.化学平衡发生移动时,化学反应速率一定变化 |
| C.正反应进行的程度越大,正反应速率一定越大 |
| D.使化学反应速率发生变化,而化学平衡不移动的影响因素,一定是催化剂 |
已知反应N2(g) + 3H2(g) 3NH3(g)ΔH < 0,能增大正反应速率的措施是
3NH3(g)ΔH < 0,能增大正反应速率的措施是
| A.通入N2 | B.扩大容器容积 | C.移去部分NH3 | D.降低体系温度 |
已知反应2M(g) + 2N(g)  xP(g) + 2Q(g),将4 mol M和2 mol N混合,充入到2 L密闭容器中,2 min后达到平衡时,生成1.6 mol P,又测得v(Q)为0.2 mol/(L·min)。下列说法正确的是
xP(g) + 2Q(g),将4 mol M和2 mol N混合,充入到2 L密闭容器中,2 min后达到平衡时,生成1.6 mol P,又测得v(Q)为0.2 mol/(L·min)。下列说法正确的是
| A.N的转化率是20% | B.x = 4 |
| C.平衡时M的物质的量为2.8 mol | D.平衡时气体总压强比原来减小 |
已知反应A  2B,A、B的浓度变化如图所示,下列反应速率正确的是
2B,A、B的浓度变化如图所示,下列反应速率正确的是
A.v(A)=" 9" mol/(L·min)B.v(B)=" 18" mol/(L·min)
C.v(A)= 4.5 mol/(L·min)D.v(B)= 4.5 mol/(L·min)