有下列物质:①乙醇②苯酚③乙醛④丙烯酸(CH2=CH—COOH)⑤乙酸乙酯,其中与溴水、酸性KMnO4溶液、NaHCO3溶液都能反应的是
A.仅①③ |
B.仅②⑤ | C.仅④ | D.仅③④ |
PCl3和PCl5都是重要的化工原料。将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:PCl3(g)+Cl2(g)  PCl5(g) △H<0。有关数据如下:
PCl5(g) △H<0。有关数据如下:
| PCl3(g) |
Cl2(g) |
PCl5(g) |
|
| 初始浓度/(mol/L) |
2.0 |
1.0 |
0 |
| 平衡浓度/(mol/L) |
(1.6)c1 |
(0.6)c2 |
0.4 |
下列判断不正确的是()
A.10 min内,v(Cl2)=0.04 mol/(L·min)
B.当容器中Cl2为1.2 mol时,反应达到平衡
C.升高温度,反应的平衡常数减小,则平衡时PCl3的转化率变大
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,
c(PCl5)<0.2 mol/L
已知乙烷的燃烧热为1190kJ/mol,则下列表述正确的是()
| A.2C2H6(g)+7O2 (g) = 4CO2 (g)+6H2O(l);△H=-1190kJ/mol |
| B.C2H6(g)+7/2O2 (g) =2CO2 (g)+3H2O(g);△H=-1190kJ/mol |
| C.298k、101kPa时,30g乙烷气体完全燃烧生成CO2气体和液态水,放出1190kJ热量; |
| D.该反应中,反应物所具有的总能量小于生成物所具有的总能量。 |
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd + 2NiOOH + 2H2O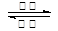 Cd(OH)2 + 2Ni(OH)2
Cd(OH)2 + 2Ni(OH)2
有关该电池的说法正确的是()
| A.充电时阳极反应:Ni(OH)2-e— + OH-="==" NiOOH + H2O |
| B.充电过程是化学能转化为电能的过程 |
| C.放电时负极附近溶液的碱性不变 |
| D.放电时电解质溶液中的OH-向正极移动 |
已知在发射卫星时可用肼(N2H4)为燃料和NO2作氧化剂,两者反应生成N2和水蒸气。
又知:N2(g)+2O2(g)===2NO2(g) ΔH=+67.7kJ·mol-1
N2H4(g)+O2(g)===N2(g)+2H2O(g)ΔH=-534kJ·mol-1
则肼与NO2反应的热化学方程式为()
| A.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(g) ΔH=+567.85kJ·mol-1 |
| B.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(g) ΔH=-567.85kJ·mol-1 |
| C.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(l) ΔH=+567.85kJ·mol-1 |
| D.N2H4(g)+NO2(g)===3/2N2(g)+2H2O(l) ΔH=-567.85kJ·mol-1 |
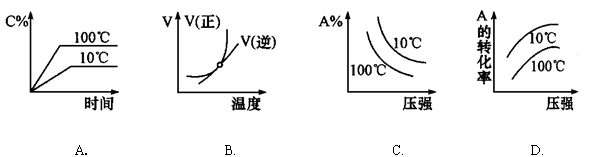
下列图像能正确地表达可逆反应3A(g) + B(g) 2C(g)(△H<0)的是()
2C(g)(△H<0)的是()