下列各组元素性质或原子结构递变情况错误的是
| A.Li、Be、B原子最外层电子数依次增多 | B.P、S、Cl元素最高正化合价依次升高 |
| C.N、O、F原子半径依次增大 | D.Li、Na、K的电子层数依次增多 |
下列物质中不能通过置换反应生成的是()
| A.S | B.CO | C.F2 | D.Fe3O4 |
下列物质的名称和化学式不相符的是()
| A.赤铁矿(Fe2O3) | B.硫铁矿(FeS2) | C.铁红(Fe2O3) | D.磁铁矿(FeO) |
下列逻辑关系图示中正确的是()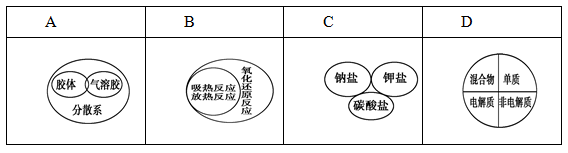
常温下,用0.1000 mol/L HCl溶液滴定20.00 mL 0.1000 mol/L NH3•H2O溶液,滴定曲线如下图。下列说法正确的是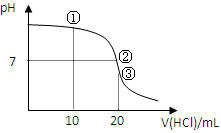
| A.①溶液:c(C1—)>c(NH4+)>c(OH—)>c(H+) |
| B.②溶液:c(NH4+)=c(C1—)>c(OH—)=c(H+) |
| C.③溶液:c(H+)>c(NH3·H2O) + c(OH—) |
| D.滴定过程中可能出现:c(NH3•H2O)>c(NH4+)>c(OH—)>c(Cl—)>c(H+) |
关于下列各实验装置的叙述中,不正确的是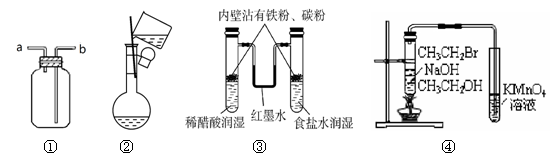
| A.装置①:a口进气可收集CO2,b口进气可收集NH3 |
| B.装置②:配制一定物质的量浓度溶液时,转移溶液 |
| C.装置③:模拟铁锈蚀 |
| D.装置④:证明CH3CH2OH发生消去反应生成了乙烯 |