下列离子方程式中正确的是
A.铜与热的浓硫酸:Cu+4H++SO42- Cu2++SO2↑+2H2O Cu2++SO2↑+2H2O |
| B.在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:NH4++OH-= NH3·H2O |
| C.用氨水吸收过量的二氧化硫:NH3·H2O+SO2=NH4++HSO3- |
| D.氯化亚铁溶液中加入稀硝酸:2Fe2++4H++NO3-=2Fe3++2H2O+NO↑ |
常温下,抽去如图所示装置中的玻璃片,使两种气体充分反应。下列说法正确的是(设NA为阿伏加德罗常数的值)( )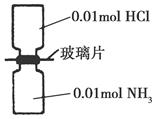
| A.反应物的总体积为0.448 L |
| B.装置中氢元素的总质量为0.04 g |
| C.生成物中含有0.01NA个分子 |
| D.生成物完全溶于水后所得溶液含有0.01NA个NH4+ |
设NA为阿伏加德罗常数的值。下列说法正确的是( )
| A.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA |
| B.78 g苯含有CC双键的数目为3NA |
| C.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA |
| D.标准状况下,6.72 L NO2与水充分反应转移的电子数目为0.1NA |
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A.常温常压下,8 g O2含有4nA个电子 |
| B.1 L 0.1 mol·L-1的氨水中有nA个NH4+ |
| C.标准状况下,22.4 L盐酸含有nA个HCl分子 |
| D.1 mol Na被完全氧化生成Na2O2,失去2nA个电子 |
某课外活动小组用如图所示装置进行实验(电解液足量)。下列说法中错误的是( )
| A.图1中,若开始实验时开关K与a连接,则B极的电极反应式为Fe-3e-=Fe3+ |
| B.图1中,若开始实验时开关K与b连接,则一段时间后向电解液中通入适量HCl气体可恢复到电解前的浓度 |
| C.图2中,若开始实验时开关K与a连接,则电解液的溶质质量分数变小 |
| D.图2中,若开始实验时开关K与b连接,则A极减少的质量等于B极增加的质量 |
某化学学习小组学习电化学后,设计了下面的实验装置图: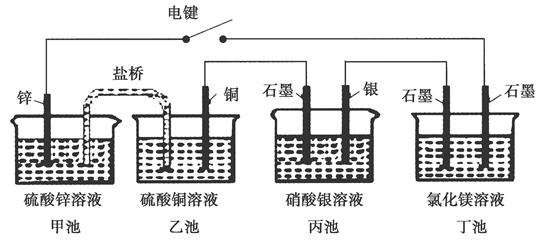
下列有关该装置图的说法中正确的是( )
| A.合上电键后,盐桥中的阳离子向甲池移动 |
| B.合上电键后,丙池为电镀银的电镀池 |
| C.合上电键后一段时间,丙池中溶液的pH增大 |
| D.合上电键后一段时间,当丙池中生成标准状况下560 mL气体时,丁池中理论上最多产生2.9 g固体 |