下列反应的离子方程式不正确的是
| A.溴化亚铁溶液中通入过量氯气2Fe2++2Br—+2C12==2Fe3++Br2+4C1— |
| B.草酸和少量烧碱溶液:H2C2O4+OH—==HC2O4—+H2O |
| C.漂白粉溶液吸收过量的二氧化碳ClO—十H2O+CO2==HClO+HCO3— |
| D.向NH4HSO4稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全 |
NH4++H++SO42-+Ba2++2OH-=NH3·H2O+BaSO4↓+H2O
在BaSO4饱和溶液中加入少量BaCl2溶液时产生沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中( )
A.c(Ba2+)=c(SO )=(Ksp) )=(Ksp)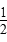 |
B.c(Ba2+)·c(SO )=Ksp,c(Ba2+)>c(SO )=Ksp,c(Ba2+)>c(SO ) ) |
C.c(Ba2+)·c(SO )>Ksp,c(Ba2+)=c(SO )>Ksp,c(Ba2+)=c(SO ) ) |
D.c(Ba2+)·c(SO )≠Ksp,c(Ba2+)<c(SO )≠Ksp,c(Ba2+)<c(SO ) ) |
下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 |
实验操作 |
现 象 |
解释或结论 |
| A |
过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 |
溶液呈红色 |
稀HNO3将Fe氧化为Fe3+ |
| B |
AgI沉淀中滴入稀KCl溶液 |
有白色沉淀出现 |
AgCl比AgI更难溶 |
| C |
Al箔插入稀HNO3中 |
无现象 |
Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D |
用玻璃棒蘸取浓氨水点到红色石蕊试纸上 |
试纸变蓝色 |
浓氨水呈碱性 |
[双选题]为了配制NH 与Cl-浓度比为1∶1的溶液,可在NH4Cl溶液中加入( )
与Cl-浓度比为1∶1的溶液,可在NH4Cl溶液中加入( )
| A.适量的HCl | B.通适量氨气 |
| C.适量的氨水 | D.适量的NaOH |
下列事实不能说明一元酸HA为弱酸的是( )
| A.常温下0.1 mol·L-1的HA溶液pH为5 |
| B.常温下NaA溶液的pH>7 |
| C.HA溶液中存在H+、OH-、A-、HA |
| D.HA溶液能与大理石反应 |
恒温下,反应aX(g)  bY(g)+cZ(g)达到平衡状态,把容器体积压缩到原来的1/2,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L,下列判断正确的是( )
bY(g)+cZ(g)达到平衡状态,把容器体积压缩到原来的1/2,且达到新的平衡状态时,X的物质的量浓度从0.1 mol/L增大到0.19 mol/L,下列判断正确的是( )
| A.a>b+c | B.a<b+c |
| C.a=b+c | D.a=b=c |