设NA为阿伏加德罗常数的值,下述正确的是
A.在Na2O2与H2O的反应中,消耗1monNa2O2转移的电 子数为2NA 子数为2NA |
| B.1L 1mol/L的碳酸钠溶液中所含阴离子的数目为NA |
| C.80g硝酸铵含有氮原子数为2NA |
| D.1L 1mol/L的盐酸溶液中,所含氯化氢分子数为NA |
热化学方程式C(s)+H2O(g)  CO(g)+H2(g);△H=+131.3kJ/mol表示( )
CO(g)+H2(g);△H=+131.3kJ/mol表示( )
| A.碳和水反应吸收131.3kJ能量 |
| B.1mol碳和1mol水反应生成一氧化碳和氢气并吸收131.3kJ热量 |
| C.1mol固态碳和1mol水蒸气反应生成一氧化碳气体和氢气,并吸热131.3kJ |
| D.1个固态碳原子和1分子水蒸气反应吸热131.1Kj |
常温下,有关水溶液pH的下列说法中正确的是
A.在pH=12的溶液中,水电离出的c(OH-) =10-2mol·L-1 =10-2mol·L-1 |
| B.将pH=2和pH=12的酸、碱溶液等体积混合后,溶液的pH=7 |
| C.若强酸、强碱中和后pH=7,则中和之前pH酸+pH碱=14 |
| D.含等物质的量的HNO3、Na2CO3、CH3COOH的溶液混合后,溶液的pH>7 |
向某NaOH溶液中通入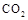 气体后得到
气体后得到 溶液M,因
溶液M,因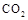 通入的量的不同,溶液M的组成也不同若
通入的量的不同,溶液M的组成也不同若 向M中加入盐酸,产
向M中加入盐酸,产 生的气体体积V(
生的气体体积V(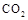 )与加入盐酸的体积V(HCl)的关系如图所
)与加入盐酸的体积V(HCl)的关系如图所 示,则下列分析与判断不正确的是(不计
示,则下列分析与判断不正确的是(不计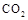 的溶解)
的溶解)
A.若OB=0,则形成溶液M所发生的离子方程为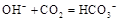 |
B.若OB=BC,则溶液M为 溶液 溶液 |
C.若OB>BC,则溶液M中大量存在的阴离子为 和 和 |
D.若3OB=BC,则溶液M中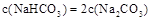 |
在含有 的溶液中,加入足量的
的溶液中,加入足量的 固体,充分反应后再加入过量的稀盐酸,溶液中离子数目不变化的是
固体,充分反应后再加入过量的稀盐酸,溶液中离子数目不变化的是
A. |
B. |
C. |
D.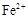 |
下列说法或表示方法正确的是
| A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
B.由C(金刚石,S)=C(石墨,S); 可知,金刚石比石墨稳定 可知,金刚石比石墨稳定 |
C.在101KPa时,2g 完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为: 完全燃烧生成液态水,放出285.8KJ热量,氢气燃烧的热化学方程式为: |
D.稀溶液中 若将含0.5mol 若将含0.5mol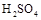 的浓溶液与含1molNaOH的溶液混合,放出的热量大于57.3KJ 的浓溶液与含1molNaOH的溶液混合,放出的热量大于57.3KJ |