(1)工业上以粗铜为原料采取如图所示流程制备硝酸铜晶体:
①在步骤a中,还需要通入氧气和水,其目的是 。
②在保温去铁的过程中,为使Fe3+沉淀完全,可以向溶液中加入CuO,调节溶液的pH,根据下表数据,溶液的pH应保持在 范围。
| |
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
| Fe3+ Cu2+ |
1.9 4.7 |
3.2 6.7 |
不用加水的方法调节溶液pH的 原因是 。
原因是 。
③进行蒸发浓缩时,要用硝酸调节溶液的pH=1,其目的是(结合离子方程式说明) 。
(2)工业上常利用硝酸铜溶液电镀铜,电镀时阴极的电极反应式是 。
(3)图-2是某小组同学 查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O ]的溶解度曲线(温度
查阅资料所绘出的硝酸铜晶体[ Cu(NO3)2·nH2O ]的溶解度曲线(温度 在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。
在30℃前后对应不同的晶体),下列说法正确的是 (填字母)。
a. A点时的溶液为不饱和溶液
b. B点时两种晶体可以共存
c. 按上述流程最终得到的晶体是Cu(NO3)2·3H2O
d. 若将C点时的溶液降温至30℃以下,可以析出Cu(NO3)2·6H2O晶体
某有机物A,由C、H、O三种元素组成,在一定条件下,A、B、C、D、E、F具有下列转化关系:
已知D的蒸气密度是氢气的29倍,并可以发生银镜反应。
(1)写出F的结构简式▲;
(2)写出C → A的反应条件▲;
(3)写出A → D的反应方程式▲。
写出B → C的反应方程式▲。
根据要求回答下列问题。
(1)分子球棍模型可以帮助人们认识有机物的结构。
下列是某有机物的分子比例模型,其中不同颜色的球代表不同的原子,球之间的“棍”
表示单键、双键或三键。
该有机物分子中可能存在的两种官能团的名称分别为 ▲、 ▲;
这类有机物在化学性质上表现的特点是 ▲。
(2)有机物的特征性质常可用以有机物之间的鉴别。
①欲区分葡萄糖和淀粉,可选用 ▲(填字母)。
A.碘水 B.银氨溶液 C.盐酸 D.NaOH溶液
②欲区分 和
和 ,可选用 ▲(填字母)。
,可选用 ▲(填字母)。
A.AgNO3溶液 B.NaOH溶液 C.FeCl3溶液 D.Na2CO3溶液
(3)同分异构现象是有机物种类繁多的原因之一。
分子式为C7H6O2的有机物有多种同分异构体,其中含有苯环和1个侧链的同分异构体的结构简式是 ▲、 ▲。
(4)高分子化合物在生产、生活中有着广泛的应用。
PES(聚丁二酸乙二醇酯)是一种生物可降解的聚酯,它在塑料薄膜,食品包装等方面有着广泛的应用。其结构简式如下:
合成PES的有机化学反应类型是 ▲反应。形成该聚合物的两种单体的结构简式分别是 ▲和 ▲。
有机物A的分子式为C3H8O,它能氧化成B,也能与浓H2SO4共热生成C。 若B不能发生银镜反应,C不能使溴水褪色,分别写出A、B、C的结构简式
下列各有机化合物都有多种官能团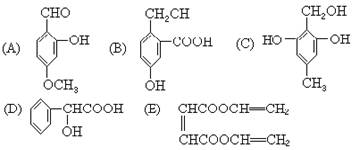
①可看作醇类的是____________________________
②可看作酚类的是____________________________
③可看作羧酸类的是__________________________
④可看作酯类的是____________________________
有机化学中取代反应的范畴很广。下列6个反应中,属于取代反应范畴的是(填写相应的字母):