下列各溶液中能大量共存的离子组是
| A.c(H+)=10-14mol/L的溶液中:Na+、A1O2-、S2-、SO32- |
| B.使pH试纸呈红色的溶液中:Fe2+、I-、NO3-、Cl- |
| C.碳酸氢钠溶液中:K+、SO42-、Cl-、H+ |
| D.使酚酞试液呈红色的溶液中:Mg2+、Cu2+、SO42-、K+ |
0.1 mol某有机物的蒸气跟过量O2混合后点燃,生成13.2 g CO2和5.4 g H2O,该有机物跟金属钠反应放出H2;又能跟新制Cu(OH)2悬浊液加热时生成砖红色沉淀,此有机物还能跟乙酸反应生成酯类化合物。该酯类化合物的结构简式可能是( )
| A.CH3CH(OCH3)CHO |
| B.OHCCH2COOCH2CH3 |
| C.CH3COOCH(CH3)CHO |
| D.CH3COOCH2CH2COCH3 |
将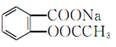 完全转变为
完全转变为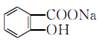 的方法为( )
的方法为( )
| A.与足量的NaOH溶液共热后,再通入CO2 |
| B.溶液加热,通入足量的HCl |
| C.与稀H2SO4共热后,加入足量的Na2CO3 |
| D.与稀H2SO4共热后,加入足量的NaOH |
0.1 mol阿司匹林其学名为乙酰水杨酸,结构简式为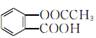 与足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )
与足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )
| A.0.1 mol | B.0.2 mol |
| C.0.3 mol | D.0.4 mol |
某中性有机物,在酸性条件下可以发生水解,生成相对分子质量相同的A和B,A是中性物质,B可以与碳酸钠反应放出气体,此有机物是( )
| A.CH3COOC3H7 | B.CH3COOC2H5 |
| C.CH3COONa | D.CH3CH2Br |
草莓、香蕉等水果具有芳香气味,是因为其中含有乙酸乙酯(化学式为C4H8O2)等物质。下列关于乙酸乙酯的说法不正确的是( )
| A.该物质属于氧化物 |
| B.乙酸与乙醇反应生成乙酸乙酯属于取代反应 |
| C.该物质的相对分子质量为88 |
| D.乙酸乙酯燃烧有二氧化碳和水生成 |