共价键、离子键和范德华力是粒子之间的三种作用力,下列晶体①Na2O2 ②SiO2
③石墨 ④金刚石 ⑤NaCl ⑥白磷中,含有两种作用力的是
| A.①②③ | B.①③⑥ | C.②④⑥ | D.①②③⑥ |
下列叙述中正确的是
| A.含有离子键的化合物一定是离子化合物 |
| B.具有共价键的化合物一定是共价化合物 |
| C.在化合物CaCl2中,两个氯离子之间也存在离子键 |
| D.化学键是分子中多个原子之间强烈的相互吸引作用 |
元素性质呈现周期性变化的基本原因是
| A.元素的原子量逐渐增大 | B.核外电子排布呈周期性变化 |
| C.核电荷数逐渐增大 | D.元素化合价呈周期性变化 |
现行元素周期表中已列出112种元素,其中元素种类最多的周期是
| A.第4周期 | B.第5周期 | C.第6周期 | D.第7周期 |
在一定温度下,4L密闭容器内存在反应 ,其中气体M、气体N的物质的量随时间变化的曲线如图所示:
,其中气体M、气体N的物质的量随时间变化的曲线如图所示: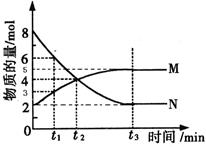
(1)比较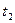 时刻,正逆反应速率大小V正V逆。
时刻,正逆反应速率大小V正V逆。
(2)若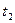 =2min,计算反应开始至
=2min,计算反应开始至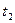 时刻,M的平均化学反应速率为:_____________________________。
时刻,M的平均化学反应速率为:_____________________________。
(3)t1与t2相比,反应速率__________较慢,其原因是__________________;已知该反应是放热反应,则N的能量___________M的能量(填“大于”、“小于”、“等于”)镁条和盐酸的总能量。
下表是元素周期表的一部分,请回答有关问题:
(1)最活泼的非金属元素是________(用元素符号或化学式表示,下同);碱性最强的是________,该物质存在的化学键类型是_________
(2)⑤元素与⑧元素形成化合物的电子式是
(3)③⑦⑧三种元素原子半径由小到大的顺序是
(4)将⑤⑥两种单质用导线相连后,同时浸入稀硫酸中,⑥这一极发生________(填“氧化”或“还原”)反应