用标准盐酸滴定未知浓度NaOH溶液时,若测定结果偏高,产生误差的原因可能是
A.滴定时,装NaOH溶 液的锥形瓶未用NaOH溶液润 液的锥形瓶未用NaOH溶液润 洗 洗 |
| B.酸式滴定管用蒸馏水洗后,用标准盐酸润洗 |
| C.滴定前,酸式滴定管尖嘴处有气泡,而在滴定后气泡消失 |
| D.滴定前仰视读取了酸式滴定管的读数,滴定后读数正确 |
自然环境与人们的生活息息相关。下列有关环境的说法不正确的是
| A.氟利昂(CCl2F2)因破坏大气臭氧层,会导致“温室效应” |
| B.生活污水中所含的氮、磷化合物是植物营养素,但会导致水体污染 |
| C.废旧电池的回收,其主要目的是为了保护环境,而不是回收金属 |
| D.淀粉餐具被认为是最有发展前景的一次性餐具,可有利于保护环境 |
下列各组分子中,都属于含极性键的非极性分子的是 ( )
| A.SO3SO2 | B.C2H4CH4 |
| C.C60 H2O2 | D.NH3 HCl |
用铅蓄电池(总反应:Pb+PbO2+4H++2SO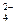
 2PbSO4;+2H2O电解苦卤水(含C1一、Br一、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。
2PbSO4;+2H2O电解苦卤水(含C1一、Br一、Na+、Mg2+)的装置如图所示(a、b为石墨电极)。
下列说法中正确的是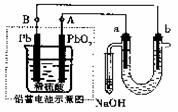
A.铅蓄电池放电时的正极反应是: PbO2+4H++SO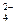 =PbSO4+2H2O =PbSO4+2H2O |
| B.电解苦卤水时,a电极首先放电的是Br一而不是Cl一,说明当其它条件相同时Br一的还原性强于Cl— |
| C.铅蓄电池充电时,A极应与外接电源负极相连 |
| D.忽略能量消耗,当b极产生0.02g气体时,铅蓄电池中消耗0.01 mol H2SO4 |
下列叙述不正确的是()
| A.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大 |
| B.一定温度下,IL 1mol/L的氨水与2L 0.5mol/L的氨水中,n(NH4+)前者多 |
| C.相同体积、相同物质的量浓度的盐酸、醋酸,稀释相同倍数后,溶液的pH:盐酸<醋酸 |
| D.0.2mol/L的一元酸HX与0.1mol/L的KOH溶液等体积混合所得溶液中,一定有:a(H+)+c(K+)=c(OH-)+c(X-) |
在体积均为1 L,pH均等于2的盐酸和醋酸中,分别投入0.12 g镁粉充分反应后,下图中比较符合反应事实的曲线是