下图为一种新型的生物燃料电池,它有两个涂覆着酶的电极,处于充满空气和少量氢气的玻璃槽中,由于气 体可以混合从而省去了昂贵的燃料隔离膜。下列对其工作原理叙述正确的是
体可以混合从而省去了昂贵的燃料隔离膜。下列对其工作原理叙述正确的是 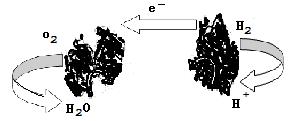
| A.该电池工作过程中,H+浓度不断增大 |
| B.该电池在高温环境下能提供更好的动力 |
| C.该电池负极反应为:H2—2e—=2H+ |
| D.该电池正极反应为O2+4e—=2O2- |
下列说法中正确的是( )
| A.水是极弱的电解质,它能微弱电离生成H+,所以严格地说纯水呈微酸性 |
| B.纯水中c(OH-)×c(H+)=Kw,Kw是一常数,不随任何条件改变而改变 |
| C.25℃时纯水中c(OH-)×c(H+)=10-14,稀酸和稀碱中Kw=c(OH-)×c(H+)≠10-14 |
D.H2O  H++OH-是吸热过程,所以温度升高,平衡向电离方向移动,KW随之增大 H++OH-是吸热过程,所以温度升高,平衡向电离方向移动,KW随之增大 |
在酸性溶液中能大量共存,并且溶液为无色透明的离子组是()
A.NH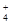 、Al3+、SO 、Al3+、SO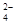 、NO 、NO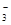 |
B.K+、Na+、CO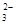 、NO 、NO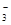 |
C.K+、NH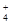 、MnO 、MnO 、SO 、SO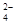 |
D.Na+、K+、NO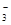 、HSO 、HSO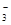 |
下列实验设计及其对应的离子方程式均正确的是( )
| A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+===Cu2++2Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2+H2O===2Na++2OH-+O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2+H2O===2H++Cl-+ClO- |
| D.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2===2Mn2++5O2↑+8H2O |
反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率v(X)(反应物的消耗速率或产物的生成速率)可表示为( )
| A.v(NH3)=0.010mol•(L•s)-1 |
| B.v(O2)=0.0010mol•(L•s)-1 |
| C.v(NO)=0.0010mol•(L•s)-1 |
| D.v(H2O)=0.045mol•(L•s)-1 |
下列有关反应限度的叙述正确的是( )
| A.大多数化学反应在一定条件下都有一定的限度 |
| B.依据焓判据:NH4HCO3受热分解可自发进行 |
| C.使用催化剂,可降低反应的活化能,加快反应速率,改变反应限度 |
| D.FeCl3与KSCN反应达到平衡时,向其中滴加KCl溶液,则溶液颜色变深 |