下列事实中,能说明氯原子得电子能力比硫原子强的是
①盐酸的酸性比氢硫酸(H2S水溶液)酸性强 ②HCl的稳定性比H2S大 ③Cl2与铁反应生成FeCl3 ,而S与铁反应生成FeS ④Cl2能与H2S反应生成S ⑤还原性:Cl-<S2-
| A.①②③④ | B.②③④ | C.①②③④⑤ | D.②③④⑤ |
下列与处理方法对应的反应方程式不正确的是
| A.工业上用水吸收NO2生产硝酸:3NO2 + H2O = 2HNO3 + NO |
| B.用氨水除去工业原料氯化铵中的氯化铁杂质:Fe3+ + 3OH- = Fe(OH)3↓ |
| C.用熟石灰处理泄漏的液氯:2Ca(OH)2 +2Cl2 = CaCl2 + Ca(ClO)2 +2H2O |
D.用明矾除去水中的悬浮颗粒物:Al3+ + 3H2O  Al(OH)3(胶体) + 3H+ Al(OH)3(胶体) + 3H+ |
食品添加剂关系到大家健康,下列物质中的添加剂作用不正确的是
| A |
B |
C |
D |
 |
 |
 |
 |
| 防治高血压 |
防治缺铁性贫血 |
做甜味剂 |
做防腐剂 |
分子式为C9H18O2的有机物A有下列转化关系:其中B、C的相对分子质量相等,则A的可能的结构简式有
A.6种 B.7种 C.8种 D.9种
某气态不饱和链烃CnHm在一定条件下与H2加成为CnHm+x,取CnHm和H2混合气体共60 mL进行实验,发现随混合气中H2所占体积的变化,反应后得到的气体总体积数也不同,反应前混合气体中H2所占的体积V(H2)和反应后气体总体积V(反应后总)的关系如图所示(气体体积均在同温同压下测定)。由此可知x的数值为
| A.4 | B.3 | C.2 | D.1 |
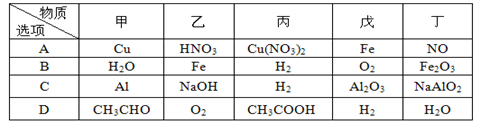
甲、乙、丙、丁、戊的相互转化关系如图所示(部分反应物及反应条件已略去,箭头表示一步转化)。下列各组物质中,满足图示转化关系的是