下列离子方程式正确的是
| A.碳酸钠加入硫酸中: Na2CO3+2H+=2Na++CO2↑+H2O |
| B.铁片加入CuSO4溶液中: 2Fe+3Cu2+=3Cu+2Fe3+ |
| C.氢氧化钠中加入盐酸: H++OH-=H2O |
| D.氯化铜溶液中加入NaOH溶液:Cu2++2OH-=Cu(OH)2↓ |
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法不正确的是
| A.充电时电极a连接电源的负极 |
| B.放电时负极的电极反应式为Zn—2e-=Zn2+ |
| C.放电时左侧电解质储罐中的离子总浓度增大 |
| D.阳离子交换膜可阻止Br2与Zn直接发生反应 |
【改编】下列反应的离子方程式正确的是
| A.FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2 = 2Fe3++Br2+4Cl- |
B.服用阿司匹林过量出现水杨酸( )中毒反应,可静脉注射NaHCO3溶液: )中毒反应,可静脉注射NaHCO3溶液: + 2 HCO3- → + 2 HCO3- → + 2 CO2↑ + 2 H2O + 2 CO2↑ + 2 H2O |
| C.强碱溶液中NaClO与Fe(OH)3反应:3ClO—+2Fe(OH)3=2FeO42—+3Cl—+H2O+4H+ |
D.FeCl3溶液中通入适量SO2,溶液黄色褪去:2Fe3++SO2 +2H2O  2Fe2+ + SO42—+ 4H+ 2Fe2+ + SO42—+ 4H+ |
【改编】用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.室温下,48.0 gO2和O3的混合气体中含有的氧原子数目为1.5NA |
| B.取2.5L 3.2 mol·L-1NaHCO3溶液 ,所得溶液含有8 NA个HCO3- |
| C.25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的Ba2+的数目为0.1NA |
| D.标准状况下,2.24 L Cl2通入足量FeCl2溶液反应,溶液颜色变黄,转移的电子总数为0.2NA |
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是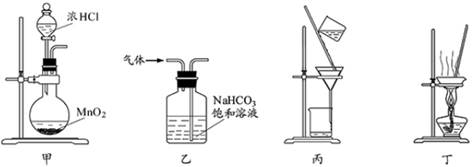
| A.用装置甲制取氯气 |
| B.用装置乙除去氯气中的少量氯化氢 |
| C.用装置丙分离二氧化锰和氯化锰溶液 |
| D.用装置丁蒸干氯化锰溶液制MnCl2·4H2O |
【改编】下列物质性质与应用对应关系正确的是
| A.加碘盐中含有碘元素,所以可以用淀粉检验真伪 |
| B.苏打具有弱碱性,可用于治疗胃酸过多引起的胃痛 |
| C.分子晶体中一定存在共价键 |
| D.铝热反应可以用来焊接钢轨 |