在某温度下,将H2和I2各0.10mol 的气态混合物充入10L的密闭容器中,充分反应,达到平衡后,测得c(H2)=" 0.0080" mol·L-1
(1)该反应的平衡常数K= (填数值)。
(2)在上述温度下,该容器中若通入H2和I2蒸气各0.20 mol,达到化学平衡状态时:
C(H2)= mol ·L-1; c(HI)= mol·L-1。
氯气在科技、生产中应用广泛。
(1)工业上常用熟石灰和氯气反应制取漂白粉,化学方程式是。
(2)实验室用MnO2与浓盐酸反应制取氯气的原理如下:MnO2 + 4HCl MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
①若制取11.2 L Cl2(标准状况),则最少应加入MnO2的质量为______g。
②用平衡移动原理解释可用排饱和食盐水法收集氯气的原因。(结合必要的化学用语及文字回答)
③制备氯气时,可用NaOH溶液吸收尾气,下列试剂也可用于吸收氯气的是____(填字母)。
a. KI溶液 b. FeCl2溶液 c. KCl溶液
写出你选择的吸收试剂与Cl2反应的离子方程式:_______。
④也可用浓氨水吸收氯气,同时生成一种无污染的气体,反应的化学方程式是_______。
桂醛在医药、化工、香料、食品等领域应用广泛。合成桂醛并用桂醛合成聚酯F的路线如下图所示。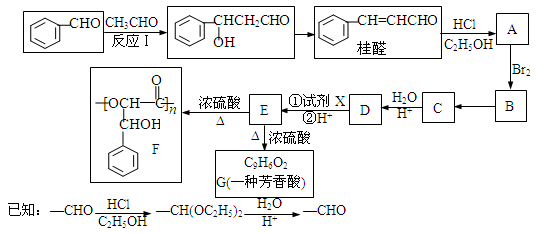
根据题意完成下列填空:
(1)写出反应类型。反应B→C;反应E→G。
(2)写出结构简式。C;G。
(3)若试剂X为新制氢氧化铜悬浊液 ,则该反应的条件是,反应现象是 _____________________ 。
(4)在浓硫酸、加热的条件下E生成F的同时有少量的G以及环酯生成,写出这种环酯一种可能的结构简式。
(5)请写出同时满足下列条件的桂醛的所有同分异构体的结构简式。
a.分子中不含醛基和羟基 b.苯的对二取代物 c.除苯环外,不含其它环状结构
(6)上述反应得到的桂醛中含有少量分子式为C11H12O2的化合物,该物质是由桂醛和乙醛发生了类似反应Ⅰ的反应生成的。写出桂醛和乙醛生成C11H12O2的化学方程式。
溴水中存在下列平衡:Br2+H2O HBr+HBrO有机反应往往比较复杂,伴随副反应发生。已知X经加成反应可能生成产物A、D,请根据下列流程填空。
HBr+HBrO有机反应往往比较复杂,伴随副反应发生。已知X经加成反应可能生成产物A、D,请根据下列流程填空。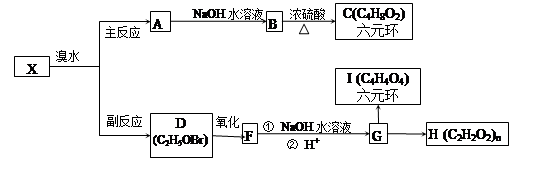
(1)A→B的反应类型为_____________,写出C的结构简式_________________;
(2)有C的同分异构体M,既能发生银镜反应,也能发生酯化反应,M有_____种同分异构体,写出其中分子结构中有支链的分子的结构简式___________________,
(3)写出下列有机物的结构简式: F_________________,I______________;
(4)完成G→H化学方程式:
__________________________________________;
(5)完成X→D化学方程式__________________________________________;
(6)X与溴水的反应中还存在一种有机副产物,其结构简式为__________________。
以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应: 2CO2(g)+6H2(g)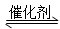 CH3CH2OH(g)+3H2O(g) -Q(Q>0)
CH3CH2OH(g)+3H2O(g) -Q(Q>0)
在密闭容器中,按H2与CO2的物质的量之比为3:1进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。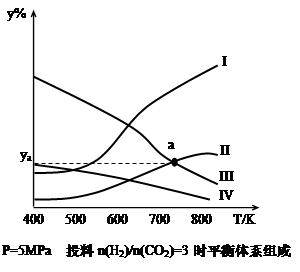
完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是_______(选填序号)
(2)在一定温度下反应达到平衡的标志是_______(选填编号)
a.平衡常数K不再增大
b.CO2的转化率不再增大
c.混合气体的平均相对分子质量不再改变
d.反应物不再转化为生成物
(3)其他条件恒定,如果想提高CO2的反应速率,可以采取的反应条件是_______(选填编号);达到平衡后,能提高H2转化率的操作是_______(选填编号)
a.降低温度 b.充入更多的H2
c.移去乙醇 d.增大容器体积
(4)图中曲线II和III的交点a对应的体积分数ya=_______%
碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛。
完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。请完成并配平上述反应:
____KI+____CuSO4 → ____I2+____Cu2I2↓+ ____________
该反应中氧化剂与还原剂的物质的量之比为___________。
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。
写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是____________________。
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为:
2Cu2I2+Hg → Cu2HgI4(玫瑰红)+ 2Cu
产物Cu2HgI4中,Cu元素显____价。
当有1 molCu2I2参与反应时,转移电子____mol。
(4)为除去稀盐酸中少量CuCl2杂质,可往溶液中加入过量的M试剂后进行过滤操作,再通入适量的Cl2后进行N操作。试剂M和操作N的组合正确的是_____(选填编号)
| 选项 |
试剂M |
操作N |
| a |
碘化钾溶液 |
升华 |
| b |
氢碘酸溶液 |
萃取分液 |
| c |
氢气 |
过滤 |
| d |
氢硫酸溶液 |
过滤 |