对下列氧化还原反应中转移电子数的判断,不正确的是
| A.H2S+H2SO4(浓)=S↓+SO2↑+2H2O:6e- |
B.3Cl2+6KOH 5KCl+KClO3+3H2O:5e- 5KCl+KClO3+3H2O:5e- |
| C.2Na2O2+2H2O=4NaOH+O2↑:2e- |
| D.2H2S+SO2=3S+2H2O:4e- |
下列说法错误的是
| A.NH4NO3溶于水虽然吸热,但其溶于水是自发过程 |
| B.加热液体(温度高于沸点)会自发转变成气体,可用焓变解释 |
| C.对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最小 |
| D.要正确判断化学反应能否自发进行,要综合考虑反应的ΔH和ΔS。 |
“活化分子”是衡量化学反应速率快慢的重要依据,下列对“活化分子”的说法中不正确的是
| A.活化分子之间的碰撞一定是有效碰撞 |
| B.增大反应物的浓度,可使单位体积内活化分子增多,反应速率加快 |
| C.对于有气体参加的反应增大压强,可使单位体积内活化分子增多,反应速率加快 |
| D.催化剂能降低反应的活化能,使单位体积内活化分子百分数大大增加 |
14CO2与碳在高温条件下发生反应:14CO2+C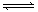 2CO,达到化学平衡后,平衡混合物中含14C的微粒有
2CO,达到化学平衡后,平衡混合物中含14C的微粒有
| A.14CO2 | B.14CO2、14CO | C.14CO2、14CO、14C | D.14CO |
下列反应中生成物总能量高于反应物总能量的是
| A.碳酸钙受热分解 | B.乙醇燃烧 |
| C.铝粉与氧化铁粉末反应 | D.氧化钙溶于水 |
关于如图所示装置的叙述,正确的是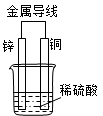
| A.铜是负极,铜片上有气泡产生 |
| B.铜片质量逐渐减少 |
| C.电流从锌片经导线流向铜片 |
| D.氢离子在铜片表面被还原 |