可逆反应:2NO2(g)  2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状 态的标志是
2NO(g)+ O2(g),在体积不变的密闭容器中反应,达到平衡状 态的标志是
① 单位时间内生成nmol O2的同时生成2nmol NO2
② 单位时间内生成nmol O2的同时生成2nmol NO
③ 用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态
④ 混合气体的颜色不再改变的状态
⑤ 混合气体的密度不再改变的状态
A .①④ B.②③⑤ C.①③④ D.①②③④⑤
.①④ B.②③⑤ C.①③④ D.①②③④⑤
下列说法正确的是()
| A.在一定条件下,乙烯能与H2发生加成反应,苯不能与H2发生加成反应 |
| B.C2H6O和C4H10都有2种同分异构体 |
| C.乙酸乙酯、乙酸均能与NaOH反应,二者分子中官能团相同 |
| D.淀粉和蛋白质均可水解生成葡萄糖 |
下列实验、现象及相关结论均正确的是()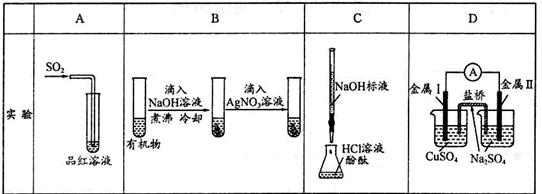
| 现象 |
品红褪色 |
最后试管有浅黄色沉淀 |
最后一滴溶液使酚酞由无色变为粉红色,且30秒不复原 |
盐桥左端从 无色逐渐变为 蓝色 |
| 结论 |
 有强 有强氧化性 |
有机物中含有溴原子 |
滴定达到终点 |
金属II比I活泼 |
关于下列各实验装置的叙述中,不正确的是()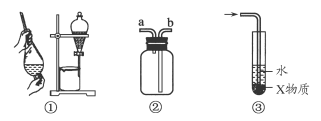
| A.装置①可用于分离C2H5OH和H2O的混合物 |
| B.装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体 |
| C.装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸 |
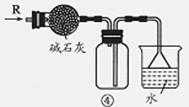
| D.装置④可用于干燥、收集NH3,并吸收多余的NH3 |
在一密闭容器中有CO、H2、O2共16.5g和足量的Na2O2,用电火花引燃,使其完全反应,Na2O2增重7.5g,则原混合气体中O2的质量分数是()
| A.54.5% | B.40% | C.36% | D.33.3% |
向CuSO4溶液中逐滴加入KI溶液至过量,观察到产生白色沉淀CuI,蓝色溶液变为棕色。再向反应后的溶液中通入过量的SO2气体,溶液变成无色。则下列说法正确的是()
| A.通入22.4 L SO2参加反应时,有2 NA个电子发生转移 |
| B.通入SO2后溶液逐渐变成无色,体现了SO2的漂白性 |
| C.滴加KI溶液时,KI被氧化,CuI是氧化产物 |
| D.上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |