某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。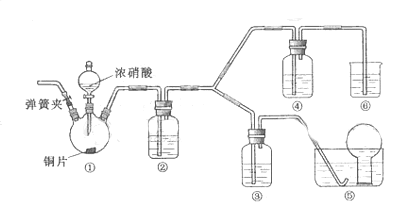
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与NO反应,能与NO2反应2NO2+2NaOH=NaNO3+NaNO2+H2O
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
(2)滴加浓硝酸之前的操作时检验装置的气密性,加入药品,打开弹簧夹后
(3)装置①中发生反应的化学方程式是
(4)装置②的作用是 ,发生反应的化学方程式是
(5)该小组得出的结论依据的试验现象是
(6)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别涉及了一下4个试验来判断两种看法是否正确。这些方案中可行的是(填序号字母,多选不给分)
a)、加热该绿色溶液,观察颜色变化 b)、加水稀释绿色溶液,观察颜色变化
c)、向该绿色溶液中通入氮气,观察颜色变化
d)、向饱和硝酸铜溶液中通入浓硝酸与铜反映产生的气体,观察颜色变化
铜与浓硝酸反应和铜与稀硝酸反应,产物不同,实验现象也不同。
⑴某课外活动小组为了证明并观察到铜与稀硝酸反应的产物为NO。设计了如图所示的实验装置。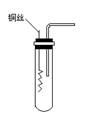
请你根据他们的思路,选择药品,完成该实验,并叙述实验步骤。
药品:稀硝酸、稀盐酸、锌粒、CaCO3固体
步骤:①检查装置的气密性;
②
③
④
⑤
⑥用注射器向广口瓶内推入氧气(或空气)
(2)推入氧气(或空气)的目的是。
(3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸的反应,所得到的溶液前者呈绿色,后者呈兰色,某同学提出这可能是Cu2+浓度差异引起的,你同意这种看法吗?(填“同意”或“不同意”),原因是。
另一同学提出溶液呈 “绿色”是Cu2+与NO2混合的结果,请你设计一个实验证明之。(简述实验方案和实验现象)。
(6分)物质的加热是中学化学实验的重要基本操作。常用加热方式有3类:①直接在酒精灯上加热;②通过石棉网用酒精灯加热;③通过水浴加热。以下10个中学化学实验中有的要加热,有的不要加热:
| A.用双氧水和二氧化锰制取氧气 |
| B.食盐溶液蒸发制取氯化钠晶体 |
| C.氯化铵与碱石灰反应制取氨气 |
| D.浓硝酸和铜反应制取二氧化氮气体 |
E.乙醇和浓硫酸制取乙烯
F.石油的分馏
G.苯与溴在铁催化下制取溴苯
H.乙醛溶液与银氨溶液发生银镜反应
I.乙酸乙酯在酸性条件下发生水解
J.葡萄糖与新制的氢氧化铜悬浊液反应
其中:
(1)可用酒精灯直接加热的有(填写字母代号,多选倒扣分,下同)。
(2)用酒精灯通过石棉网加热的有。
(3)通常用水浴加热的有。
如图,某同学做乙醇氧化实验时将螺旋状铜丝先放到a点处加热,然后再移到b点,发现铜丝在火焰的a,b两点时现象明显不同,请写出a,b两点的实验现象,并解释产生该现象的原因.
| 实验现象 |
解 释 |
|
| a |
||
| b |
(16分)某天然碱的化学组成可能为aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数),为确定其组成,化学兴趣小组的同学进行了如下实验:
(1)定性分析
①取少量天然碱样品放入试管中,用酒精灯加热,在试管口有液体生成,该液体能使无水硫酸铜变蓝。能否说明样品中含结晶水,试简述理由。
②请你设计一个简单的实验方案,确认样品中含有CO32—离子。
(2)定量分析
该小组同学设计了下图所示装置,测定天然碱的化学组成。
A B C D E
实验步骤:
①按上图(夹持仪器未画出)组装好实验装置后,首先进行的操作是。
A处碱石灰的作用是。
②称取天然碱样品7.3g,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶的质量为 87.6g,装碱石灰的U型管D的质量为74.7g。
③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟。
④关闭活塞K1、K2,打开K3,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后称得装浓硫酸的洗气瓶质量为88.5g;装碱石灰的U型管D的质量为75.8g。该步骤中缓缓鼓入空气数分钟的目的是
。
计算推导:
该天然碱的化学式为。
(6分)(1)指出下列实验用品或仪器(已经洗涤干净)使用时的第一步操作:
①石蕊试纸(检验气体性质);
②容量瓶。
(2)下列有关化学实验操作中“先”与“后”的说法正确的是(填代号)。
| A.用排水法收集气体后,先移出导管,后撤酒精灯 |
| B.给试管加热时,先均匀加热,后局部加热 |
| C.碱液流到桌子上,先用稀醋酸溶液中和,后用水洗 |
| D.浓硫酸不慎洒到皮肤上,先迅速用水冲洗,后涂上3%-5%的NaHCO3溶液 |
E.点燃可燃性气体(如H2、CO、C2H4等)时,都要先检验气体纯度,后点燃