 燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是
燃料电池(DBFC)的结构如右图,有关该电池的说法正确的是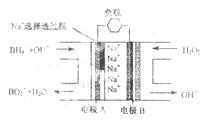
A. 电极B为负极
B. 电池负极区的电极反应为:
C. 放电过程中,Na+从正极区向负极区迁移
D. 在电池反应中,每消耗1 L 6moH.L-1 H2O2溶液,理论上流过电路中的电子为6NA
如图装置进行实验,将液体A逐滴加入到固体B中,下列叙述正确的是( )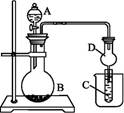
| A.若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色 |
| B.若A为醋酸,B为贝壳,C中盛氯化钙溶液,则C中溶液变浑浊 |
| C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生白色沉淀后沉淀溶解 |
| D.实验仪器D可以起到防止溶液倒吸的作用 |
下列制取物质的方案中,最合理的是( )
| A.用过量的铁与稀硫酸反应制绿矾(FeSO4·7H2O) |
| B.铜与浓硫酸反应制CuSO4 |
| C.过量的Fe与Cl2反应制FeCl2 |
| D.MnO2与稀盐酸反应制Cl2 |
下图是实验室制备CO2的简易装置图。用该装置制备CO2可起到随时使反应发生或停止的效果。选项中装置可起到与右图装置相同效果的是( )

下列制取气体的方案,可以直接采用如图所示装置进行的是( )
①用H2O2和MnO2制取O2 ②用CaCO3和稀盐酸制取CO2 ③用KClO3和MnO2制取O2 ④用Zn和稀硫酸制取H2 ⑤用Cu和浓硝酸制取NO2
| A.①④ | B.②③④ | C.①②⑤ | D.①②④⑤ |
用下图所示装置(必要时可加热试管),不能完成的实验是( )
| A.试管中盛酚酞溶液,验证氨气的水溶液呈碱性 |
| B.试管中盛酸性高锰酸钾溶液,探究SO2的还原性 |
| C.试管中盛稀氢氧化钠溶液,验证CO2与NaOH反应的产物 |
| D.试管中盛淀粉KI溶液,验证氯气的氧化性 |