如图,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准)。则下列有关说法正确的是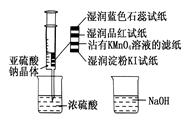
| A.蓝色石蕊试纸先变红后褪色 |
| B.品红试纸、沾有KMnO4溶液的滤纸均褪色证明了SO2具有漂白性 |
| C.湿润淀粉KI试纸变蓝说明SO2的氧化性弱于I2 |
| D.NaOH溶液可用于除去实验中多余的SO2 |
将下列各种单质投入或通入CuSO4溶液中,能产生铜单质的是( )
| A.Fe | B.Na | C.H2 | D.Ag |
下列有关金属的说法正确的是( )
| A.生铁与钢的区别在于生铁含碳杂质,而钢不含 |
| B.铜在自然界中的含量高,所以铜是人类最早使用的金属 |
| C.黑色金属材料包括铁、铬、锰及其化合物 |
| D.金属一般都具有导电性、导热性、延展性 |
下列试剂保存或盛放方法正确的是( )
| A.浓硝酸盛放在铜质器皿中 |
| B.稀硝酸盛放在铁质器皿中 |
| C.NaOH溶液保存在带橡胶塞的试剂瓶中 |
| D.NaOH溶液保存在带玻璃塞的试剂瓶中 |
检验氨气可选用( )
| A.湿润的蓝色石蕊试纸 | B.干燥的红色石蕊试纸 |
| C.干燥的蓝色石蕊试纸 | D.湿润的红色石蕊试纸 |
可用来干燥氨气的有( )
| A.浓硫酸 | B.碱石灰 |
| C.氯化钙 | D.五氧化二磷 |