某烃的衍生物1.45g,跟足量银氨溶液反应后析出5.4g银,则该有机物的结 构简式是
构简式是
| A.CH3CHO | B.CH3CH2CHO | C.CH2OH(CHOH)4CHO | D.CH3CH2CH2OH |
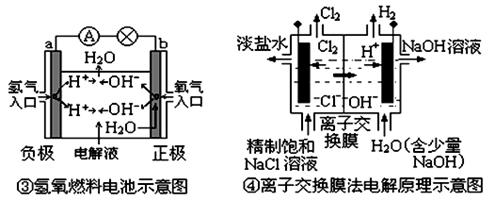
观察下列几个装置示意图,有关叙述正确的是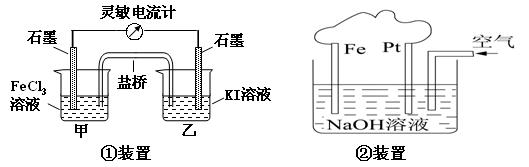
| A.①装置的总反应为2Fe3++2I-=2Fe2++I2 |
| B.②装置中Fe为阴极,电极反应为 Fe-2e-+ 2OH-=Fe(OH)2 |
| C.③装置中外电路电子由b极流向a极 |
| D.④装置的离子交换膜允许阳离子、阴离子、水分子自由通过 |
下列离子方程式正确的是
A.Ag2S沉淀溶解平衡表达式:Ag2S  2Ag+ + S2- 2Ag+ + S2- |
| B.硫代硫酸钠溶液和稀硫酸反应:SO42--+S2O32-+6H+=3SO2↑+3H2O |
| C.碳酸氢钠溶液与足量的氢氧化钡溶液混合:HCO3-+Ba2++OH- = BaCO3↓+H2O |
| D.酸性高锰酸钾与草酸反应:MnO4-+H2C2O4+2H+=MnO2+2CO2↑+2H2O |
NA代表阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,11.2L氯仿中含有C-Cl键的数目为1.5NA |
| B.pH=2、体积为1L的醋酸溶液中含醋酸分子的数目为0.01NA |
| C.7.8g Na2O2 晶体中阴、阳离子总数为0.3NA |
| D.常温常压下,17g甲基(—14CH3)所含的中子数为9NA |
某合作小组讨论辨析以下说法不正确的是
| A.粗盐和酸雨都是混和物 | B.沼气和水煤气都是可再生能源 |
| C.不锈钢和目前流通的硬币都是合金 | D.豆浆和雾都是胶体 |
某烃含碳、氢原子物质的量之比为1∶2,该烃对氮气的相对密度为2,该烃可使溴水褪色,该烃与氢气加成的产物的二氯代物有三种同分异构体.该烃为
| A.CH2=CH—CH2—CH3 | B.CH2=CH—CH3 |
| C.CH2=C(CH3)2 | D.环丁烷 |