碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以KOH溶液为电解液,电池总反应式为:Zn(s) + 2MnO2(s) + H2O(l)===Zn(OH)2(s) + Mn2O3(s)。下列说法正确的是( )
| A.该电池的正极为锌 |
| B.电池正极的反应式为:2MnO2(s) + H2O(1) + 2e— ="==" Mn2O3(s) + 2OH—(aq) |
| C.电池工作时,电子由正极通过外电路流向负极 |
| D.该电池反应中二氧化锰起催化作用 |
下列各组物质的性质及粒子的性质变化正确的是
| A.稳定性H2S>HCl>HBr>HI | B.酸性HF>HCl>HBr>HI |
| C.离子半径K+>Cl->S2->S | D.酸性HClO4>H2SO4>H2CO3>HClO |
主族元素X、Y、Z的常见离子为aX+、bY2—、cZ—,半径大小关系是X+<Z—<Y2—下列说法不正确的是
| A.b一定小于c | B.单质的氧化性Z > Y |
| C.Y2—的还原性大于Z— | D.X、Y可处于同周期或X在Y的下周期 |
汽车的启动电源常用铅蓄电池,该电池在放电时的反应如下:
Pb (s)+ PbO2(s) +2H2SO4(aq) 2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是()
2PbSO4(s) +2H2O(l),根据此反应判断下列叙述中正确的是()
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb(s)+SO42-(aq)–2e – = PbSO4(s) |
| C.铅蓄电池属于一次电池 |
| D.电池放电时,溶液酸性增强 |
下表为元素周期表前四周期的一部分,且X、Y、Z、R和W为主族元素。下列说法正确的是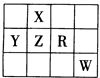
| A.五种元素可能都是金属元素 |
| B.五种元素的原子最外层电子数一定都大于2 |
| C.X的氢化物的沸点一定比Z的氢化物的沸点高 |
| D.R的最高价氧化物对应的水化物一定是强酸 |
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是
| A.原子半径:W> Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.4种元素的单质中,Z单质的熔、沸点最低 |
| D.W单质能与水反应,生成一种具有漂白性的物质 |