转基因食品的安全性目前已成为人们争论的焦点之一,但这样并不能阻止转基因技术应用于生产实践的种种尝试,转基因小牛的诞生就是其中的一例。
人的血清白蛋白在临床上需求量很大,通常从人血中提取。由于艾滋病病毒(HIV)等人类感染性病原体造成的威胁与日俱增,使人们对血液制品顾虑重重。如果应用基因工程和克隆技术,将人们的血清白蛋白基因导入乳牛细胞中,那么利用牛的乳汁生产血清白蛋白就成为可能。大致过程如下:
| A.将人的血清白蛋白基因导入雌奶牛胚胎细胞,形成重组细胞① |
| B.取出重组细胞①的细胞核,注入去核牛卵细胞中形成重组细胞② |
| C.电脉冲刺激重组细胞②,促使其形成早期胚胎 |
| D.将胚胎移植到母牛的子宫中,最终发育成转基因小牛。 |

(1)重组细胞①是通过转基因技术,实现了奶牛胚胎细胞中的DNA与_______________重组。
(2)重组细胞②是通过___________工程中的_____________技术,使重组细胞①的细胞核与去核牛卵细胞的细胞质融合。
(3)若将早期的胚胎分离成若干个胚胎细胞。让其分别发育成一头小牛,这些小牛的基因型________(完全相同. 部分相同.完全不同),这是因为________________________。
(4)利用转基因牛乳汁提取药物工艺简单,甚至可直接饮用治病。如果将药物蛋白基因移到动物如牛的膀胱上皮细胞中,利用转基因牛尿液生产提取药物比乳汁提取药物有更大优越性:处于不同发育时期的 性动物都可生产药物。
下图中,图1是某种生物细胞的亚显微结构示意图,图2为此细胞相关生理过程示意图,请据图回答: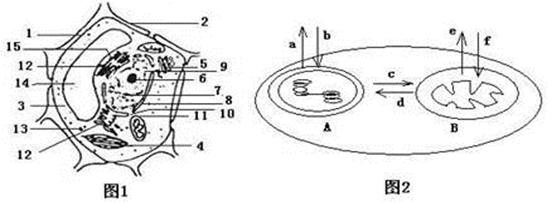 (1) 1的结构特点是。若图1所示细胞是根尖分生区细胞,则图中不该有的细胞器是和(用图中数字表示)。
(1) 1的结构特点是。若图1所示细胞是根尖分生区细胞,则图中不该有的细胞器是和(用图中数字表示)。
(2)在细胞有丝分裂过程中,周期性重建和消失的匀质球形小体是[ ](括号内填数字,横线上填结构名称)。
(3)图中4和11两种结构的作用分别是,。
(4)比较11中内、外膜的蛋白质的含量,可发现内膜的蛋白质的含量明显高于外膜,原因主要是。上图中的几种生物膜中,在细胞中分布最广泛的是[ ](注意:15为核糖体,请在括号内填数字,横线上填结构名称)。
(5)在光照比较强时,图1中磷酸含量最低的场所是_____(填结构名称)。
(6)若4产生的气体被11利用,要穿过层生物膜;在较强的光照条件下,B产生的CO2主要去向是图中的途径(用图中的字母表示)。在A和B中都会产生[H],但其产生的场所和功能是不同的:在A中产生[H]的场所是,功能是;在B中产生[H]的场所是,功能是。在A中,ATP的运动方向是;在B中,[H]的运动方向是。
下图一表示某种膜结构以及物质进出膜方式,图二表示某细胞在进行分泌蛋白的合成和分泌前几种生物膜的面积。请据图回答:
(1)图一中大写字母B和 C分别表示___________和___________。
(2)若图一为红细胞膜,则图中箭头[]表示钾离子的吸收过程。
(3)请在图二中画出细胞在进行分泌蛋白的合成和分泌后这几种生物膜的面积变化。
(4)在合成旺盛的细胞内,可与内质网膜直接相连的生物膜有________________________
(5)透析型人工肾中的血液透析膜检测了生物膜的__________性。
分析ATP与ADP相互转化的示意图,回答下列问题:
(1)图中Pi代表磷酸,则B为____________,C为____________。
(2)E不是物质,在人和动物体内E1来自______,绿色植物体内则来自____________。
(3)在植物体的生命活动中,E2主要用于___________、_____________等生命活动。
(4)A1和 A2相同吗?____。根据你的分析,它们的作用分别是_______________。
下列是某化合物的结构简图,据图回答:
(1)此化合物的名称是______________,含有个—NH2,个—COOH。
(2)图中含有肽键个,肽键可表示为;图中表示R基的代号是______。
(3)形成该化合物的生物化学反应叫做____,在这个过程中,相对分子质量减少了_____。
(4)组成这类化合物的基本单位的结构通式是________________。
回忆课本中的实验,回答有关实验的问题:
(1)检测生物组织中的糖类、脂肪或蛋白质的存在,可以根据它们与某些化学试剂所产生的颜色反应,来检测物质的种类。检测组织样液中蛋白质的存在可用试剂,呈现的颜色为。
(2)提取叶绿体中的色素的有机溶剂是。叶绿素主要吸收————————————光
(3)利用紫色洋葱表皮细胞进行质壁分离和复原实验时,观察到表皮细胞已经发生了质壁分离,请描述液泡的变化为。(变大或变小)
(4)观察洋葱根尖有丝分裂时解离的目的——————————
(5)在探究pH值对酶活性的影响实验中,实验的自变量是(2分)