实验室中制取氢气,最好的方法是
| A.纯锌与稀硫酸反应 | B.纯锌与浓硫酸反应 |
| C.纯锌与稀盐酸反应 | D.粗锌(含铜、银)与稀硫酸反应 |
已知:
①N2(g)+O2(g)="==2NO(g)" ΔH1=+180 kJ·mol-1
②N2(g)+3H2(g)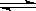 2NH3(g) ΔH2=-92.4 kJ·mol-1
2NH3(g) ΔH2=-92.4 kJ·mol-1
③2H2(g)+O2(g)===2H2O(g) ΔH3=-483.6 kJ·mol-1
下列说法正确的是
| A.反应②中的能量变化如图所示,则ΔH2=E1-E3 |
| B.H2的燃烧热为241.8 kJ·mol-1 |
| C.氨的催化氧化反应为4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH=+906 kJ·mol-1 |
| D.由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 |
温度为25 ℃时,将0.23 g钠投入到100 g水中充分反应,假设反应后溶液体积为100 mL,则该溶液的pH为
| A.1 | B.10 | C.12 | D.13 |
反应Fe(s)+CO2(g) FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是
FeO(s)+CO(g),700 ℃时平衡常数为1.47,900 ℃时平衡常数为2.15。下列说法正确的是
| A.升高温度该反应的正反应速率增大,逆反应速率减小 |
B.该反应的化学平衡常数表达式为K= |
| C.该反应的正反应是吸热反应 |
| D.增大CO2浓度,平衡常数增大 |
在密闭容器中进行反应:X2(g)+Y2(g)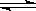 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.3 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
| A.Z为0.3 mol·L-1 | B.Y2为0.4 mol·L-1 |
| C.X2为0.2 mol·L-1 | D.Z为0.4 mol·L-1 |
对反应A+B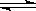 AB来说,常温下按以下情况进行反应:
AB来说,常温下按以下情况进行反应:
①20 mL溶液中含A、B各0.01 mol
②50 mL溶液中含A、B各0.05 mol
③0.1 mol·L-1的A、B溶液各10 mL
④0.5 mol·L-1的A、B溶液各50 mL
四者反应速率的大小关系是
A.②>①>④>③ B.④>③>②>①
C.①>②>④>③ D.①>②>③>④