在体积一定的密闭容器中给定物质A、B、C的量,在一定条件下发生反应建立的化学平衡:
aA(g) + bB(g)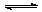 xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表
xC(g),符合下图所示的关系(c%表示平衡混合气中产物C的百分含量,T表
示温度,p表示压强)。在图中,Y轴是指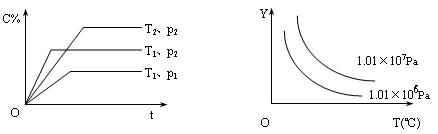
A.反应物A的百分含量 B.平衡混合气中物质B的百分含量
C.平衡混合气的密度 D.平衡混合气的平均摩尔质量
探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是
| A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水 |
| B.将pH=11的氨水稀释1000倍,测得pH > 8,说明NH3·H2O为弱碱 |
| C.加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明NH4HCO3受热不稳定 |
| D.将红热的Pt丝伸入上图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的氧化产物为NO2 |
某药物中间体X,其结构如图所示。下列说法正确的是
| A.X分子中含有手性碳原子 |
| B.X可发生氧化、消去、取代等反应 |
| C.X既能与盐酸反应,又能与NaOH溶液反应 |
| D.1mol X与H2反应,最多消耗4mol H2 |
下列有关说法正确的是
| A.马口铁(镀锡铁皮)镀层破损后铁仍不易腐蚀 |
B.CH3Cl(g)+Cl2(g) CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0 CH2Cl2(l)+HCl(g)能自发进行,则该反应的ΔH>0 |
| C.MnS悬浊液中滴加少量CuSO4溶液可生成CuS沉淀,则Ksp(CuS)< Ksp(MnS) |
| D.合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率 |
已知:(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1
(2)C(s)+O2(g)=CO2(g) △H2
(3)2H2(g)+O2(g)=2H2O(l) △H3
(4)2CO2(g)+4H2(g)=CH3COOH(l)+2H2O(l) △H4
(5)2C(s)+2H2(g)+O2(g)=CH3COOH(l) △H5
下列关于上述反应的焓变的判断正确的是
| A.△H1>0,△H2<0 | B.△H5=2△H2+△H3-△H1 |
| C.△H3>0,△H5<0 | D.△H4=△H1-2△H3 |
短周期主族元素X、Y、W、Z、R的原子序数依次增大。其中X、Z同主族,Z的单质是一种良好的半导体材料,W3+与Y2-具有相同的核外电子数,R是同周期中原子半径最小的元素。下列叙述正确的是
| A.Y2-的离子半径大于W3+的离子半径 |
| B.Y、Z形成的化合物为离子化合物 |
| C.W的最高价氧化物对应的水化物的酸性比X的强 |
| D.Z的气态简单氢化物的稳定性比R的强 |