关于反应:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O说法不正确的是
MnCl2+Cl2↑+2H2O说法不正确的是
| A.反应中氧化剂与还原剂物质的量之比为1:2 |
| B.要使8.7g MnO2完全反应,需投入含0.4molHCl的浓盐酸 |
| C.每生成标准状况下2.24L Cl2,就有7.3gHCl被氧化 |
| D.若有0.4molHCl被氧化,反应中转移的电子数为0.4×6.02×1023 |
元素性质呈现周期性变化的根本原因是( )
| A.元素的相对原子质量递增,量变引起质变 |
| B.元素原子的核外电子排布呈周期性变化 |
| C.元素的原子半径呈周期性变化 |
| D.元素的化合价呈周期性变化 |
下列说法正确的是( )
| A.离子化合物中只能含有离子键 |
| B.共价化合物中可能含有离子键 |
| C.化学键存在于分子之间 |
| D.化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程 |
某元素原子的原子核外有三个电子层,最外层电子数是4,该原子核内的质子数是( )
| A.14 | B.15 | C.16 | D.17 |
下列各组粒子中属于同位素的是( )
| A.16O和18O | B.H2O和D2O | C.H2和D2 | D.24Mg和24Na |
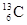 -NMR(核磁共振)可用于含碳化合物的结构分析,
-NMR(核磁共振)可用于含碳化合物的结构分析,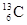 表示的是( )
表示的是( )
| A.核外有13个电 子,其中6个能参与成键 |
| B.核内有6个质子,核外有7个电子 |
| C.质量数是13,原子序数是6,核内有7个质子 |
| D.质量数是13,原子序数是6,核内有7个中子 |