25℃时,水的电离可达到平衡:H2O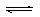 H++OH- △H>0,下列叙述正确的是
H++OH- △H>0,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,Kw增大,pH不变 |
在F、P、S三种元素中,每种元素都有某些方面区别于其他两种元素;若从中选出氟元素,选择的理由是()
| A.单质与冷水反应非常剧烈 | B.单质固态时属于分子晶体 |
| C.一定条件下,能与氢气发生化合反应 | D.最高价氧化物对应的水化物是强酸 |
下列性质中,可以证明某化合物内一定存在离子键的是()
| A.晶体可溶于水 | B.具有较高的熔点 |
| C.水溶液能导电 | D.熔融状态能导电 |
下列各分子中,所有原子都满足最外电子层上有8电子的结构的是()
| A.H2O | B.PCl3 | C.SO2 | D.BF3 |
根据相关化学原理,下列判断正确的是()
A.若X是原子晶体,Y是分子晶体,则熔点:X<Y
B.若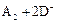 ═
═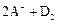 ,则氧化性:D2>A2
,则氧化性:D2>A2
C.若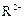 和
和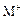 的电子层结构相同,则原子序数:R<M,离子半径:
的电子层结构相同,则原子序数:R<M,离子半径: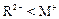
D.若弱酸HA、HB的酸性HA>HB,则溶液的碱性NaA>NaB
实现下列变化时,需克服相同类型作用的是()
| A.纯碱和烧碱的熔化 | B.水晶和干冰的熔化 |
| C.食盐和冰醋酸的熔化 | D.液溴和液汞的气化 |