下列图中所示的实验操作正确的是 ( )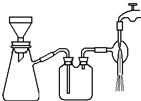

| A.从溶液中分离出KNO3晶体 | B.除去Cl2中的HCl 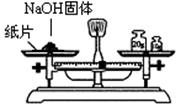 |
| C.锌、铜、硫酸铜溶液原电池 | D.用托盘天平快速称量 |
由短周期元素组成的中学常见物质A、B、C、D、E、X,存在下图转化关系 (部分生成物和反应条件略去)。下列推断不正确的是()
A.若D与盐酸反应,可生成A和B,则X一定是H2O
B.若D是一种强碱,则A、B、C 均可与X反应生成D
均可与X反应生成D
C.若D为NaCl,且A可与C反应生成B,则E可能是CO2
D.若D是一种强酸,则A既可以是单质,也可以是化合物,且D可与铜反应生成B或C
某溶液中只含有Na+、H+、OH-、A-四种离子,下列说法正确的是
A.若c(OH-)>c(H+),溶液中不可能存在:c(Na+)>c(OH-)>c(A-)>c(H+)
B.溶液中不可能存在:c(Na+)>c (A-)>c(OH-)>c(H+)
C.若溶液中c(A-) = c(Na+),则溶液一定呈中性
D.若溶质为NaA、HA,则一定存在: c(A-)>c(Na+)>c(H+)>c(OH-)
下列说法错误的是
| A.食醋用氢氧化钠溶液滴定开始时,溶液的pH通常变化缓慢,当接近完全反应时(即滴定终点),pH出现突变,称为滴定突跃。 |
| B.Cu2+与足量氨水反应的离子方程式 Cu2++2NH3·H2O==Cu(OH)2↓+2NH4+ |
| C.抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快。 |
| D.硝酸钾饱和溶液冷却未出现结晶时,可以用玻璃棒充分磨擦器皿壁促使晶体析出。 |
海洋中有丰富的食品、矿产,能源、药物和水产资源等(如下图所示),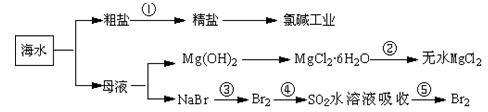
下列有关说法正确的是
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→Ba Cl2溶液→过滤后加盐酸 Cl2溶液→过滤后加盐酸 |
B.第②步中结晶出的MgCl2·6H2 O可在空气中受热分解制无水MgCl2 O可在空气中受热分解制无水MgCl2 |
| C.在第③④⑤步中溴元素均被氧化 |
| D.从第③步到第⑤步的目的是为了浓缩 |
下列叙述正确的是
| A.48 g O3气体含有6.02×1023个O3分子 |
| B.常温常压下,4.6 gNO2气体含有1.81×1023个NO2分子 |
| C.0.5 mol·L-1L CuCl2溶液中含有3.01×1023个Cu2+ |
| D.标准状况下,22.4 L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |