元素性质随着原子序数的递增呈现周期性变化的原因是:
| A.元素原子的核外电子排布呈周期性变化 | B.元素原子的电子层数呈周期性变化 |
| C.元素原子半径呈周期性变化 | D.元素的化合价呈周期性变化 |
Cu—Zn稀硫酸组成原电池装置,当导线中有0.5mol电子通过时,理论上两极的变化是
①锌极反应:Zn-2e-=Zn2+,锌片上产生0.25mol的H2
②铜极反应:2H++2e-=H2↑,锌片溶解16.25g
③电流由铜极经导线流向锌极 ④溶液中SO42-移向铜极
| A.①④ | B.③④ | C.②③ | D.①③ |
NA代表阿伏加德罗常数的值,下列有关叙述正确的是
| A.1mol乙烷(CH3CH3)中含有共价键的数目为6NA |
| B.由CO2和O2组成的混合气体共有NA个分子,其中氧原子数为2NA |
| C.标准状况下,22.4LH2O中含氢原子数为2NA |
| D.制取84消毒液(NaClO),消耗0.5mol氯气转移电子数为NA |
下列有关化学用语表述正确的是
A.CO2的电子式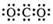 |
B.Cl-的结构示意图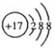 |
| C.次氯酸的结构式 H-Cl-O | D.质量数为37的氯原子 17 37Cl |
为除去括号内的杂质,所选用的试剂或方法不正确的是
| A.NaHCO3溶液(Na2CO3溶液) 通入过量的CO2 |
| B.铁粉(铝粉) 加入适量的NaOH溶液过滤 |
| C.Na2CO3溶液(Na2SO4溶液) 加入适量的Ba(OH)2溶液过滤 |
| D.CO2 (CO) 将混合气体通过足量灼热的CuO |
下列实验操作中错误的是
| A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,分液漏斗下层液体应从下口放出,上层液体应从上口倒出 |
| D.萃取操作时,所选萃取剂溶解溶质能力应大于原溶剂且与原溶剂互不相溶 |